题目内容
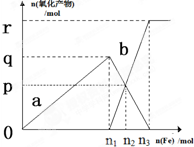 含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )
含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )| A、a是Fe(NO3)2 |
| B、n1=0.80 |
| C、p=0.60 |
| D、n3=1.20 |
考点:化学方程式的有关计算
专题:计算题
分析:向稀硝酸中加入铁粉时,开始先生成Fe(NO3)3,当铁过量时,过量的铁再与 Fe(NO3)3反应生成 Fe(NO3)2,反应涉及两个方程式.
解答:
解:向稀硝酸中加入铁粉时,发生两个过程,开始先生成Fe(NO3)3,反应方程式为:Fe+4 HNO3(稀)=Fe(NO3)3+NO↑+2H2O,根据硝酸的物质的量为4mol利用方程式可计算出生成的 Fe(NO3)3为1mol,所以参加反应的铁为1mol即n1=1,a为 Fe(NO3)3,故AB错误;
C.Fe(NO3)3 与过量的铁继续反应生成 Fe(NO3)2,反应方程式为:2Fe(NO3)3+Fe=3 Fe(NO3)2,P点为 Fe(NO3)3 与 Fe(NO3)2物质的量相等的点,设生成的 Fe(NO3)2物质的量xmol,则利用方程式可求得x=0.6,即P=0.6,故C正确;
D.再根据铁原子守恒,n(Fe)=n(Fe((NO3)2)+n (Fe(NO3)),所以 n(Fe)=1.2mol即n2=1.2mol,所以n3大于1.2,故D错误;
故选C.
C.Fe(NO3)3 与过量的铁继续反应生成 Fe(NO3)2,反应方程式为:2Fe(NO3)3+Fe=3 Fe(NO3)2,P点为 Fe(NO3)3 与 Fe(NO3)2物质的量相等的点,设生成的 Fe(NO3)2物质的量xmol,则利用方程式可求得x=0.6,即P=0.6,故C正确;
D.再根据铁原子守恒,n(Fe)=n(Fe((NO3)2)+n (Fe(NO3)),所以 n(Fe)=1.2mol即n2=1.2mol,所以n3大于1.2,故D错误;
故选C.
点评:本题考查了铁与稀硝酸的反应,要注意铁和硝酸谁多谁少,以及加入的顺序.

练习册系列答案
相关题目
将15g两种金属的混合物投入足量的盐酸中,反应完全后得到H2 11.2L(标准状况)该混合物的组成可能是( )
| A、钠和铁 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
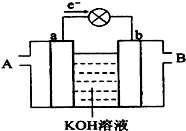 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L |
下列实验中,不能达到相应实验目的是( )
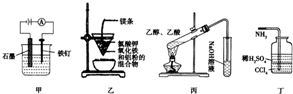

| A、装置甲:防止铁钉生锈 |
| B、装置乙:可制得金属铁 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:吸收多余的氨气 |
用一种试剂就能鉴别出乙醛、乙酸、乙醇、甲酸,此试剂是( )
| A、银氨溶液 |
| B、新制的Cu(OH)2 悬浊液 |
| C、溴水 |
| D、碳酸钠溶液 |
化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A、阿司匹林具有解热镇痛作用 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 |
| D、石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 |
下列关于电解质的电离平衡状态的叙述中,正确的是( )
| A、弱电解质的电离达到平衡状态后,电离就停止了 |
| B、分子的消耗速率和离子的生成速率相等,说明弱电解质的电离达到平衡状态 |
| C、弱电解质的电离达到平衡状态后,分子和离子的浓度相等 |
| D、弱电解质的电离达到平衡状态后,外界条件改变,电离平衡可能要发生移动 |