题目内容
下列离子方程式书写正确的是( )
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、将少量二氧化碳通入烧碱溶液中:CO2+OH-=HCO3- |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至刚好沉淀完全:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、NaHCO3溶液与NaHSO4溶液混合:HCO3-+H+=H2O+CO2↑ |
考点:离子方程式的书写
专题:
分析:A.向CaCl2溶液中通入少量CO2气体,不反应;
B.少量二氧化碳通入烧碱溶液,生成碳酸钠和水;
C.至刚好沉淀完全,生成硫酸钡、水、NaOH;
D.反应生成硫酸钠、水、二氧化碳.
B.少量二氧化碳通入烧碱溶液,生成碳酸钠和水;
C.至刚好沉淀完全,生成硫酸钡、水、NaOH;
D.反应生成硫酸钠、水、二氧化碳.
解答:
解:A.向CaCl2溶液中通入少量CO2气体,不反应,不能写离子反应,故A错误;
B.将少量二氧化碳通入烧碱溶液中的离子反应为CO2+2OH-═CO32-+H2O,故B错误;
C.向Ba(OH)2溶液中滴加NaHSO4溶液至刚好沉淀完全的离子反应为Ba2++OH-+H++SO42-=BaSO4↓+H2O,故C错误;
D.NaHCO3溶液与NaHSO4溶液混合的离子反应为HCO3-+H+=H2O+CO2↑,故D正确;
故选D.
B.将少量二氧化碳通入烧碱溶液中的离子反应为CO2+2OH-═CO32-+H2O,故B错误;
C.向Ba(OH)2溶液中滴加NaHSO4溶液至刚好沉淀完全的离子反应为Ba2++OH-+H++SO42-=BaSO4↓+H2O,故C错误;
D.NaHCO3溶液与NaHSO4溶液混合的离子反应为HCO3-+H+=H2O+CO2↑,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、与量有关的离子反应考查,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B、若用50 mL 0.55 mol?L-1的氢氧化钠溶液,分别与50 mL 0.50 mol?L-1的盐酸和50 mL0.50mol?L-1硫酸充分反应,两反应的中和热不相等 |
| C、0.2 mol/L HCl溶液与等体积0.05 mol/L Ba(OH)2 溶液混合后,溶液的pH=1 |
| D、0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO32-)+c(OH-) |
在下列各溶液中,一定能大量共存的离子组是( )
| A、常温下pH=7的溶液中:Fe3+、Na+、Cl-、SCN- |
| B、常温下c(OH-)/c(H+)=1014的溶液中:K+、Mg2+、Cl-、Br- |
| C、含有大量HCO3-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| D、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+ |
下列说法不正确的是( )
| A、钠块可用小刀切割,说明钠质地柔软 |
| B、铝制餐具不能长期存放酸性食物,但可长期存放碱性食物 |
| C、金属钠着火时,用细沙覆盖灭火 |
| D、KAl(SO4)2溶于水的电离方程式为:KAl(SO4)2═K++Al3++2SO42- |
仅改变下列一个条件,不是通过提高活化分子的百分率来提高反应速率的是( )
| A、加压 | B、加热 | C、催化剂 | D、光照 |
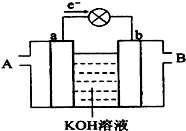 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L |