题目内容
18.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
| A. | ①表示2molC(s)燃烧生成2molCO(g)需要吸收221 kJ的热量 | |
| B. | 碳的燃烧热大于110.5 kJ/mol | |
| C. | 稀硫酸与浓NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
分析 A.该反应的焓变为负值,为放热反应;
B.燃烧热是1mol可燃物完全燃烧生成稳定氧化物反应放出的热量;
C.中和热是强酸强碱的稀溶液反应生成1mol水放出的热量;
D.醋酸是弱酸存在电离平衡,电离过程是吸热反应.
解答 解:A.反应热化学方程式分析可知是放热反应,焓变为负值,①表示2mol C(s)燃烧生成2mol CO(g)需要放出221kJ的热量,故A错误;
B.燃烧热是1mol可燃物完全燃烧生成稳定氧化物反应放出的热量,碳的燃烧热大于 110.5kJ/mol,故B正确;
C.中和热是强酸强碱的稀溶液反应生成1mol水放出的热量,稀硫酸与浓NaOH溶液反应,浓氢氧化钠溶液溶解放热,反应放出的热量大于中和热,反应的中和热为△H<-57.3kJ/mol,故C错误;
D.醋酸是弱酸存在电离平衡,电离过程是吸热反应,稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3kJ,故D错误;
故选B.
点评 本题考查反应热与焓变,题目难度不大,涉及燃烧热、中和热概念的分析判断,注意弱电解质电离平衡过程是吸热过程,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
5.化学基本概念及原理在化学反应中应用广泛.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
已知△H2=+41kJ•mol-1,则△H3=-220kJ•mol-1;平衡常数K3=$\frac{{K}_{1}}{{K}_{2}}$(用K1、K2表示).
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.
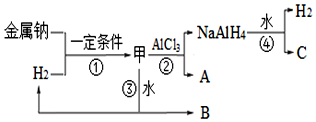
①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 745 | 465 | 413 |
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.

①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.
6.下列关于有机化合物的说法不正确的是( )
| A. | 1,2-二甲苯也称邻二甲苯 | |
| B. | 氨基乙酸与a-氨基丙酸的混合物一定条件下脱水能生成4种二肽 | |
| C. | 苯与溴水不能发生加成反应,所以两者混合后无明显现象 | |
| D. | C5H10O2属于羧酸的同分异构体有4种 |
13.丙烯在一定条件下发生加聚反应的产物是( )
| A. | 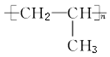 | B. | 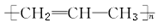 | ||
| C. | 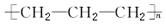 | D. | 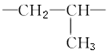 |
3.下列说法正确的是( )
| A. | 常温常压下,22.4L Cl2中含有的分子数为6.02×1023个 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的pH减小 | |
| C. | 氢氧燃料电池工作时,H2在负极上失去电子 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强 |
10.已知C(s)+H2O(g)═CO(g)+H2(g)△H=a kJ•mol-1
2C(s)+O2(g)═2CO(g)△H=-220kJ•mol-1,H-H、O═O和O-H的键能分别为436kJ•mol-1、496kJ•mol-1和462kJ•mol-1,则a为( )
2C(s)+O2(g)═2CO(g)△H=-220kJ•mol-1,H-H、O═O和O-H的键能分别为436kJ•mol-1、496kJ•mol-1和462kJ•mol-1,则a为( )
| A. | -332 | B. | -118 | C. | 350 | D. | 130 |
8.${\;}_{16}^{35}$S可用于治疗软骨肉瘤,下列关于${\;}_{16}^{35}$S的说法错误的是( )
| A. | 质量数35 | B. | 中子数19 | C. | 核电荷数35 | D. | 质子数16 |