题目内容
3.下列说法正确的是( )| A. | 常温常压下,22.4L Cl2中含有的分子数为6.02×1023个 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的pH减小 | |
| C. | 氢氧燃料电池工作时,H2在负极上失去电子 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强 |
分析 A.没有说明是否是标准状况下;
B.加热促进盐的水解;
C.原电池中负极失电子;
D.加水稀释溶液中离子浓度减小.
解答 解:A.没有说明是否是标准状况下,无法求出物质的量,故A错误;
B.0.1mol/LNa2CO3溶液加热后,碳酸根离子的水解程度增大,碱性增强,溶液的pH增大,故B错误;
C.氢氧燃料电池工作时,H2在负极上失去电子,氧气在正极上得电子,故C正确;
D.加水稀释溶液中离子浓度减小,所以稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱,故D错误;
故选C.
点评 本题考查了有关物质的量的计算、盐的水解、溶液的导电性,题目难度不大,注意应用气体摩尔体积的条件,侧重于考查学生的分析能力和应用能力.

练习册系列答案
相关题目
10.下列溶液中与50mL 1mol•L-1的AlCl3溶液中氯离子浓度相等的是( )
| A. | 150 mL 2 mol•L-1的NaCl | B. | 75 mL 2 mol•L-1的NH4Cl | ||
| C. | 150 mL 3 mol•L-1的KCl | D. | 75 mL 2 mol•L-1的CaCl2 |
18.已知反应:
①101kPa时,2C(s)+O2(g)═2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)═2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
| A. | ①表示2molC(s)燃烧生成2molCO(g)需要吸收221 kJ的热量 | |
| B. | 碳的燃烧热大于110.5 kJ/mol | |
| C. | 稀硫酸与浓NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
13.下列化学用语表示正确的是( )
| A. | 甲烷的球棍模型: | |
| B. | 硫离子的结构示意图: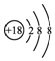 | |
| C. | HF的电子式:H:F | |
| D. | 氯酸钾的电离方程式:KClO3═K++ClO3- |
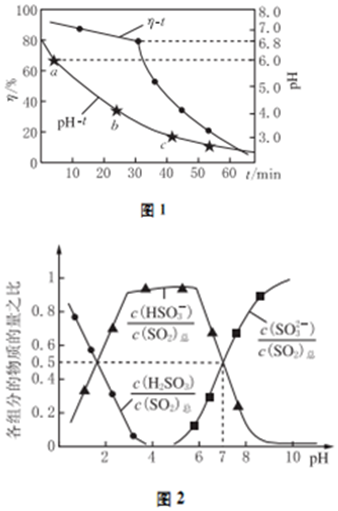
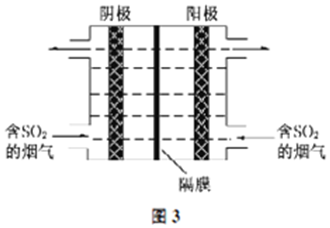
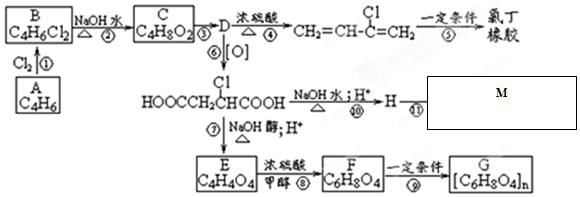

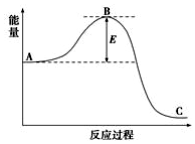 工业合成氨N2(g)+3H2(g)?2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题:
工业合成氨N2(g)+3H2(g)?2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题: