题目内容
下列有关Na2CO3和NaHCO3性质的比较中,正确的是( )
| A、热稳定性:Na2CO3<NaHCO3 |
| B、将Na2CO3与NaHCO3分别加入到足量的同物质的量浓度稀盐酸中,产生气体的快慢:Na2CO3>NaHCO3 |
| C、Na2CO3和一定量的HCl反应时,改变反应物的滴加顺序,反应现象肯定不同,产生气体的量(相同条件下)可能相同也可能不同;而NaHCO3 和一定量的HCl反应时,改变反应物的滴加顺序,反应现象与产生气体的量(相同条件下)均相同 |
| D、25℃时在水中的溶解度:Na2CO3<NaHCO3 |
考点:钠的重要化合物
专题:元素及其化合物
分析:A.碳酸氢钠受热易分解生成碳酸钠和水、二氧化碳;
B.相同条件下NaHCO3比Na2CO3反应放出气体剧烈;
C.依据碳酸钠与盐酸反应首先生成碳酸氢钠,然后碳酸氢钠与盐酸反应生成二氧化碳;
D.依据碳酸钠溶解度大于碳酸氢钠判断.
B.相同条件下NaHCO3比Na2CO3反应放出气体剧烈;
C.依据碳酸钠与盐酸反应首先生成碳酸氢钠,然后碳酸氢钠与盐酸反应生成二氧化碳;
D.依据碳酸钠溶解度大于碳酸氢钠判断.
解答:
解:A.碳酸氢钠受热易分解生成碳酸钠和水、二氧化碳,所以热稳定性:Na2CO3>NaHCO3,故A错误;
B.碳酸钠与盐酸反应首先生成碳酸氢钠,然后碳酸氢钠与盐酸反应生成二氧化碳,所以相同条件下NaHCO3比Na2CO3反应放出气体剧烈,产生气体的快慢:Na2CO3<NaHCO3,故B错误;
C.碳酸钠中滴入盐酸,开始碳酸根离子与氢离子反应生成碳酸氢根离子,无气体生成,盐酸中滴入碳酸钠溶液,直接反应生成二氧化碳,如果盐酸不足,则两种情况下产生二氧化碳不足,如果盐酸足量产生二氧化碳相同;碳酸氢钠与盐酸反应,反应实质都是氢离子与碳酸氢根离子反应生成二氧化碳,改变反应物的滴加顺序,对反应不产生影响,故C正确;
D.碳酸钠溶解度大于碳酸氢钠,故D错误;
故选:C.
B.碳酸钠与盐酸反应首先生成碳酸氢钠,然后碳酸氢钠与盐酸反应生成二氧化碳,所以相同条件下NaHCO3比Na2CO3反应放出气体剧烈,产生气体的快慢:Na2CO3<NaHCO3,故B错误;
C.碳酸钠中滴入盐酸,开始碳酸根离子与氢离子反应生成碳酸氢根离子,无气体生成,盐酸中滴入碳酸钠溶液,直接反应生成二氧化碳,如果盐酸不足,则两种情况下产生二氧化碳不足,如果盐酸足量产生二氧化碳相同;碳酸氢钠与盐酸反应,反应实质都是氢离子与碳酸氢根离子反应生成二氧化碳,改变反应物的滴加顺序,对反应不产生影响,故C正确;
D.碳酸钠溶解度大于碳酸氢钠,故D错误;
故选:C.
点评:本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意把握Na2CO3和盐酸反应的实质是解题关键.

练习册系列答案
相关题目
下列除杂方法不正确的是(括号内为杂质)( )?
| A、H2(H2S)通过CuSO4溶液洗涤? |
| B、SO2(SO3)通过饱和NaHSO3溶液洗涤? |
| C、Na2SO3溶液(Na2SO4)滴加适量的BaCl2溶液? |
| D、Na2SO4溶液(Na2SO3)滴加适量的H2SO4溶液? |
下列关于碳酸钠与碳酸氢钠性质的比较中,正确的是( )
| A、常温时的水溶性:Na2CO3<NaHCO3 |
| B、等物质的量时与足量酸反应产生CO2的量:Na2CO3>NaHCO3 |
| C、与等浓度稀盐酸反应的快慢:Na2CO3<NaHCO3 |
| D、同质量时消耗盐酸的量:Na2CO3<NaHCO3 |
下列说法正确的是( )
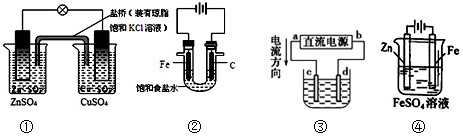

| A、图①铜锌原电池工作时,盐桥中的K+移向ZnSO4溶液 |
| B、图②装置反应一段时间,将湿润的KI淀粉试纸靠近碳电极管口,试纸变蓝 |
| C、用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
| D、用装置④可进行铁片镀锌 |
根据对角线原则,Be和Al的化学性质相似,下列说法正确是( )
| A、BeCl2溶液 pH>7,将其蒸干,灼烧后可得到BeCl2晶体 |
| B、BeCl2溶液能导电,说明BeCl2一定是离子化合物 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、Be只能与盐酸反应,不能与NaOH溶液反应 |
氧化还原反应实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-═NO↑+2H2O,KMnO4、Na2CO3、Cu2O、FeSO4四种物质中有物质(甲)能使上述还原过程发生.则下列说法中正确的是( )
| A、在上述反应中,电子从氧化剂转移到还原剂 |
| B、物质甲可能是KMnO4 |
| C、反应中若产生3.0g气体,则转移电子数约为0.3×6.02×1023 |
| D、氧化过程的反应式一定为Cu2O-2e-+2H+═2Cu2++H2O |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、0.l mol?L-1的NaAlO2溶液:K+、Na+、SO42-、CO32- |
| B、使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- |
| C、含有大量ClO-溶液中:K+、OH-、I-、SO32- |
| D、c(Al3+)=0.1 mol?L-1的溶液中:Na+、Cl-、AlO2-、SO42- |
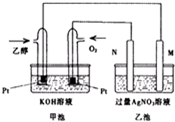 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: