题目内容
氧化还原反应实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-═NO↑+2H2O,KMnO4、Na2CO3、Cu2O、FeSO4四种物质中有物质(甲)能使上述还原过程发生.则下列说法中正确的是( )
| A、在上述反应中,电子从氧化剂转移到还原剂 |
| B、物质甲可能是KMnO4 |
| C、反应中若产生3.0g气体,则转移电子数约为0.3×6.02×1023 |
| D、氧化过程的反应式一定为Cu2O-2e-+2H+═2Cu2++H2O |
考点:氧化还原反应
专题:
分析:要使硝酸根离子发生还原反应,则需要加入还原剂,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中KMnO4具有强氧化性,Na2CO3没有氧化性和还原性,Cu2O有还原性,所以能使硝酸根离子发生还原反应的是Cu2O,二者反应生成硝酸铜、NO和水,反应方程式为14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O,该反应中N元素的化合价降低,Cu元素的化合价升高;FeSO4也具有还原性,可发生类似的反应,以此来解答.
解答:
解:A.氧化剂得到电子,还原剂失去电子,故A错误;
B.KMnO4具有强氧化性,与硝酸根离子不反应,故B错误;
C.反应中若产生3.0g气体,转移电子为
×(5-2)=0.3mol,则转移电子数约为0.3×6.02×1023,故C正确;
D.Cu2O、FeSO4均可发生氧化反应,若为Cu2O,则可能的反应为Cu2O-2e-+2H+═2Cu2++H2O,故D错误;
故选C.
B.KMnO4具有强氧化性,与硝酸根离子不反应,故B错误;
C.反应中若产生3.0g气体,转移电子为
| 3.0g |
| 30g/mol |
D.Cu2O、FeSO4均可发生氧化反应,若为Cu2O,则可能的反应为Cu2O-2e-+2H+═2Cu2++H2O,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握物质的性质及元素化合价变化为解答的关键,侧重氧化还原反应基本概念及分析、应用能力的考查,题目难度不大.

练习册系列答案
相关题目
下列有关Na2CO3和NaHCO3性质的比较中,正确的是( )
| A、热稳定性:Na2CO3<NaHCO3 |
| B、将Na2CO3与NaHCO3分别加入到足量的同物质的量浓度稀盐酸中,产生气体的快慢:Na2CO3>NaHCO3 |
| C、Na2CO3和一定量的HCl反应时,改变反应物的滴加顺序,反应现象肯定不同,产生气体的量(相同条件下)可能相同也可能不同;而NaHCO3 和一定量的HCl反应时,改变反应物的滴加顺序,反应现象与产生气体的量(相同条件下)均相同 |
| D、25℃时在水中的溶解度:Na2CO3<NaHCO3 |
下列说法正确的是( )
| A、由一种元素组成的物质可能是混合物 |
| B、同一主族不同元素的最高价氧化物,晶体结构一定相同 |
| C、最外层电子数为1的元素一定是主族元素 |
| D、由非金属元素组成的化合物一定是共价化合物 |
下列金属中,一定条件下既能跟Cl2反应,又能跟稀盐酸反应,且均生成MCl2型化合物的是( )
| A、Al | B、Fe | C、Cu | D、Mg |
100mL 2mol?L-1稀盐酸与一定量的锌充分反应,锌全部溶解,生成的氢气在标准状况下体积为1.12L,设反应后溶液的体积仍为100mL,则反应后溶液中H+物质的量浓度为( )
| A、1.5 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、0.25 mol?L-1 |
从同一瓶盐酸溶液中取任意体积时,下列物理量不随所取体积的多少而变化的是( )
| A、溶液中HCl的物质的量 |
| B、溶液的浓度 |
| C、溶液中Cl-的数目 |
| D、溶液的质量 |
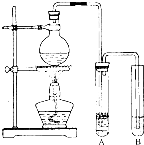 实验室制取少量溴乙烷的装置如图.
实验室制取少量溴乙烷的装置如图.