题目内容
16.据探测月球土壤中吸附着数百万吨可作为核聚变材料的${\;}_{2}^{3}$He.下列有关${\;}_{2}^{3}$He的说法正确的是( )| A. | 质量数为2 | B. | 质子数为2 | C. | 质子数为3 | D. | 质量数为1 |
分析 原子符号中左上角为质量数,左下角为质子数,原子中核电荷数=质子数=核外电子数,质量数=质子数+中子数.
解答 解:${\;}_{2}^{3}$He的质子数为2,质量数为3,故选B.
点评 本题考查了原子符号的表示意义,掌握基础是解题关键,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
7.将 4mol A 气体和 2mol B 气体在 2L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若经 2s (秒)后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质A的转化率为70% | |
| D. | 2 s 时物质B的浓度为1.4 mol•L-1 |
4.波士顿大学的研究学者用HCOOH、H2S、NH3、CO2、H2O、NH4HCO3、N2等物质,借助计算机模拟原始的新陈代谢,以支持“现代生物源自矿物地球化学”这一观点.下列说法正确的是( )
| A. | H2S沸点比H2O高 | B. | NH3和CO2均属于弱电解质 | ||
| C. | NH3(l)气化为NH3(g)放出热量 | D. | HCOOH能与NH4HCO3反应放出CO2 |
11. 英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
 英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )| A. | 该装置能够在高温下工作 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 装置工作时,电能转变为化学能 | |
| D. | 装置工作时,电子由电极a沿导线流向电极b |
1.下列各组物质中,化学键类型相同,晶体类型也相同的是( )
| A. | Cl2和 KCl | B. | SiO2 和 CO2 | C. | CH4和 H2O | D. | KCl和 HCl |
8.设NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 将1molNH4NO3于稀氨水便溶液呈中性,溶液中NH4+数目为NA | |
| B. | 标准状况下,22.4L甲烷中含有的C-H键数目为3NA | |
| C. | 25℃时,pH=2的硫酸溶液中含有H+的数目为0.01NA | |
| D. | 1molFe与1molCl2充分反应转移电子数为3NA |
5.下列叙述不正确的是( )
| A. | 糖类、油脂、蛋白质都是高分子化合物 | |
| B. | 淀粉遇碘溶液变蓝 | |
| C. | 正丁烷和异丁烷互为同分异构体 | |
| D. | 天然气的主要成分是甲烷 |
5.下表是25℃时三种弱酸的电离平衡常数:
回答下列问题:
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)NaHCO3的电离方程式是NaHCO3=Na++HCO3-.
(3)A-、CO32-、HCO3-在水中结合H+的能力由大到小的顺序为CO32->A->HCO3->NO2-.
(4)25℃时,等物质的量浓度的HA和NaA的混合溶液呈碱性,则该混合溶液中各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),解释HA和NaA的混合溶液呈碱性的原因A-离子水解程度大于HA电离程度.
(5)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(6)某同学用Na2CO3和NaHCO3溶液进行如图所示实验.
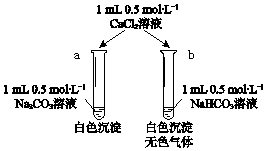
①充分反应后a试管中大量存在的离子是Na+、Cl-.
②用离子方程式表示b试管中发生的反应2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
| 化学式 | HA(A代表某种酸根) | HNO2 | H2CO3 |
| Ka | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)NaHCO3的电离方程式是NaHCO3=Na++HCO3-.
(3)A-、CO32-、HCO3-在水中结合H+的能力由大到小的顺序为CO32->A->HCO3->NO2-.
(4)25℃时,等物质的量浓度的HA和NaA的混合溶液呈碱性,则该混合溶液中各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),解释HA和NaA的混合溶液呈碱性的原因A-离子水解程度大于HA电离程度.
(5)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(6)某同学用Na2CO3和NaHCO3溶液进行如图所示实验.

①充分反应后a试管中大量存在的离子是Na+、Cl-.
②用离子方程式表示b试管中发生的反应2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.

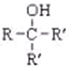
 .写出同时满足下列条件的B的同分异构体的结构简式
.写出同时满足下列条件的B的同分异构体的结构简式 .
. ,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为
,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为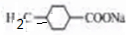 .
.