题目内容
15.如图所示为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图.下列说法正确的是( )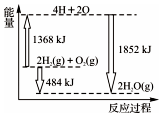
| A. | H2(g)和O2(g)反应生成H2O(g),这是个吸热过程 | |
| B. | 由2 mol H2和1 mol O2变成4 mol H、2 mol O原子,这是个放热过程 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 KJ能量 | |
| D. | 4 mol H、2 mol O生成2 mol H2O(g),共放出484 KJ能量 |
分析 由图象可知反应物总能量大于生成物总能量,为放热反应,化学反应时,断裂化学键吸收能量,形成化学键放出能量,以此解答该题.
解答 解:A.氢气与氧气的能量比水的能量高,反应放热,故A错误;
B.从图上可见4mol H、2mol O原子能量高,断键吸热,故B错误;
C.从图上可知,2mol H2(g)和1mol O2(g)反应生成2mol H2O(g),共放出484kJ能量,故C正确;
D.4mol H、2mol O生成2mol H2O(g),共放出1852KJ能量,故D错误;
故选C.
点评 本题考查了反应能量变化、图象分析数据计算应用,为高频考点,题目难度中等,侧重于基础知识的考查,考查学生的分析能力和计算能力.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
13.下列物质的分子中,键角最小的是( )
| A. | NH3 | B. | SO3 | C. | H2O | D. | CCl4 |
10.下列化学用语表达正确的是( )
| A. | HClO的电子式 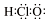 | B. | 丙烷分子的比例模型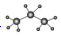 | ||
| C. | 对氯甲苯的结构简式 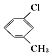 | D. | 乙醇的分子式C2H6O |
20.下列说法不正确的是( )
| A. | 冶炼金属时,必须加入一种物质作还原剂 | |
| B. | 利用金属活泼性的不同,可以采用不同的冶炼方法 | |
| C. | 湿法炼铜和火法炼铜的反应中,铜元素都发生还原反应 | |
| D. | 人类历史上大量生产和使用铝、铁、铜三种金属单质的时间顺序是铜、铁、铝 |
7.将 4mol A 气体和 2mol B 气体在 2L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若经 2s (秒)后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质A的转化率为70% | |
| D. | 2 s 时物质B的浓度为1.4 mol•L-1 |
4.波士顿大学的研究学者用HCOOH、H2S、NH3、CO2、H2O、NH4HCO3、N2等物质,借助计算机模拟原始的新陈代谢,以支持“现代生物源自矿物地球化学”这一观点.下列说法正确的是( )
| A. | H2S沸点比H2O高 | B. | NH3和CO2均属于弱电解质 | ||
| C. | NH3(l)气化为NH3(g)放出热量 | D. | HCOOH能与NH4HCO3反应放出CO2 |
5.下列叙述不正确的是( )
| A. | 糖类、油脂、蛋白质都是高分子化合物 | |
| B. | 淀粉遇碘溶液变蓝 | |
| C. | 正丁烷和异丁烷互为同分异构体 | |
| D. | 天然气的主要成分是甲烷 |

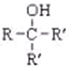
 .写出同时满足下列条件的B的同分异构体的结构简式
.写出同时满足下列条件的B的同分异构体的结构简式 .
. ,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为
,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为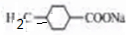 .
.