题目内容
1.在10L恒容密闭容器中充入X(g)和Y(g).发生反应X(g)+Y(g)?M(g)+N(g),所得实验数据如表:| 实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| A. | 实验①中,若5min时测得n(M)=0.050mol,则0~5min时间内,用N表示的平均反应速率v(N)=l.0×10-2 mo1•L-1•min-1 | |
| B. | 实验②中,该反应的平衡常数K=2.0 | |
| C. | 实验③中,达到平衡时,X的转化率为60% | |
| D. | 该反应的正反应方向为吸热反应 |
分析 A、根据v=$\frac{△c}{△t}$计算v(M),在利用速率之比等于化学计量数之比计算v(N);
B、由表中数据,利用三段式计算平衡时其它组分的物质的量,由于反应中气体的化学计量数相等,可以用物质的量代替浓度代入平衡常数表达式计算;
C、温度不变平衡常数不变,根据平衡常数可求出转化量,进而求出转化率;
D.对比实验①②的平衡常数可知,正反应为放热反应.
解答 解:A.v(N)=v(M)=$\frac{△c}{△t}$=$\frac{0.05mol}{10L×5min}$=1.0×10-3mol/(L•min),故A错误;
B. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.01 0.04 0 0
转化浓度(mol/L) 0.008 0.008 0.008 0.008
平衡浓度(mol/L) 0.002 0.032 0.008 0.008
实验②中,该反应的平衡常数K=$\frac{c(M)c(N)}{c(X)c(Y)}$=$\frac{0.008×0.008}{0.002×0.032}$=1.0,故B错误;
C. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.02 0.03 0 0
转化浓度(mol/L) $\frac{a}{10}$ $\frac{a}{10}$ $\frac{a}{10}$ $\frac{a}{10}$
平衡浓度(mol/L)0.02-$\frac{a}{10}$ 0.03-$\frac{a}{10}$ $\frac{a}{10}$ $\frac{a}{10}$
该反应的平衡常数K=$\frac{c(M)c(N)}{c(X)c(Y)}$=$\frac{\frac{a}{10}×\frac{a}{10}}{(0.02-\frac{a}{10})(0.03-\frac{a}{10})}$=1.0,解得a=0.12,实验③中,X的转化率=$\frac{0.12}{0.2}$×100%=60%,故C正确;
D.根据三段式可求得,700℃时,
X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.04 0.01 0 0
转化浓度(mol/L) 0.009 0.009 0.009 0.009
平衡浓度(mol/L) 0.031 0.001 0.009 0.009
K=$\frac{0.009×0.009}{0.031×0.001}$=2.6
化学平衡常数K≈2.6,升高温度至800℃得平衡常数为K=1.0,K减小,即平衡逆向移动,则正反应为放热反应,对比实验①②的平衡常数可知,正反应为放热反应,故D错误;
故选C.
点评 本题考查化学反应速率、化学平衡常数、化学平衡的影响因素分析和计算等,注意数据的分析判断,题目难度中等.

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案| A. | X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 | |
| B. | Y元素最高价氧化物对应的水化物化学式为H2YO4 | |
| C. | 原子半径由大到小的顺序为Z>Y>W | |
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
| A. | 原子半径:Y>Z>X>W | |
| B. | 气态氢化物的热稳定性:Y<Z | |
| C. | 简单阴离子的还原性:Y>X | |
| D. | 最高价氧化物对应的水化物的酸性:Z>Y |
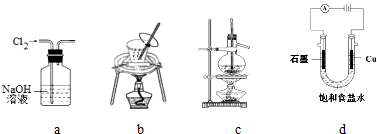
| A. | 用图a所示装置除去Cl2中含有的HCl | |
| B. | 用图b所示装置从饱和食盐水中提取氯化钠 | |
| C. | 用图c所示装置制取乙烯气体 | |
| D. | 用图d所示装置制取Cl2、H2 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向AgCl悬浊液中加入NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
| C | 向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| D | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 | |
| B. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| C. | SiCl4在战争中常用作烟雾弹,是因为它水解时生成白色烟雾 | |
| D. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
| 实验装置 | 电解质溶液 | 实验现象 | |
 | 5mol/L NaCl溶液 | a极附近 | b极附近 |
| 开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
| ①氯化亚铜(CuCl)为白色粉末,微溶于水; ②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的Cu2O; ③Cu+水溶液中不稳定,酸性条件下易歧化为Cu2+和Cu; ④氢氧化铜可以溶于浓NaOH得到蓝色溶液. |
(2)同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是Cu-e-+Cl-=CuCl↓.
(3)①橙黄色沉淀中含有Cu2O,则CuCl转化为Cu2O的原因是CuCl+OH-=CuOH+Cl-、2CuOH=Cu2O+H2O(用方程式表示);
②结合离子在溶液中的运动规律,解释“a极附近沉淀自下而上”变为橙黄色原因是通电时,在阴极产生的OH-向阳极定向移动.
(4)同学们通过实验进一步证实沉淀中含有$\stackrel{+1}{Cu}$:将橙黄色沉淀滤出洗涤后,滴加0.2mol/L H2SO4至过量,应观察到的现象是沉淀溶解,溶液变蓝,且有少量红色固体产生.
(5)同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为$\stackrel{+1}{Cu}$.为此,他们用Cu电极电解5mol/L NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀.
根据现象能否得出“该猜想不成立”的结论,并说明理由:不能,阳极产生的大量O2可能将CuOH氧化.
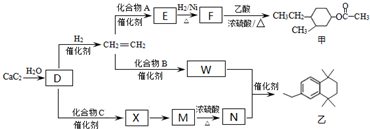
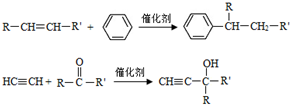 (-R、-R′代表烃基或-H)
(-R、-R′代表烃基或-H)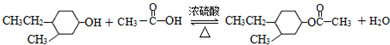 .
.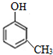 .
.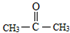 .
.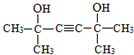 .
.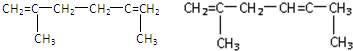 .
.