题目内容
2. X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子的未成对电子数在同周期元素中最多,W形成的单质是空气的主要成分之一,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子的未成对电子数在同周期元素中最多,W形成的单质是空气的主要成分之一,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:(1)Q+核外电子排布式为1s22s22p63s23p63d10;
(2)化合物YX4中Y的杂化方式为sp3,ZW3-离子的立体构型是平面三角形.
(3)Y、R的最高价氧化物的沸点较高的是SiO2(填化学式),原因是SiO2为原子晶体,CO2为分子晶体.
(4)Q元素可形成一种化合物[Q(NH3)4]SO4,该物质中含化学键有配位键,极性共价键,离子键.
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为8,Y原子的配位数为4,若晶胞的边长为a pm,晶体的密度为ρg/cm3,则阿伏加德罗常数的数值为$\frac{{96×{{10}^{30}}}}{{{a^3}•ρ}}$(用含a和ρ的代数式表示)
分析 X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,则X为H元素;Y有三个能级,且每个能级上的电子数相等,核外电子排布为1s22s22p2,故Y为C元素;R与Y同一主族,结合原子序数可知,R为Si,而Z原子单电子数在同周期元素中最多,则外围电子排布为ns2np3,原子序数小于Si,故Z为N元素;W形成的单质是空气的主要成分之一,则W为O元素;Q的最外层只有一个电子,其他电子层电子均处于饱和状态,不可能为短周期元素,原子序数小于30,故核外电子排布为1s22s22p63s23p63d104s1,则Q为Cu元素,以此解答该题.
解答 解:X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,则X为H元素;Y有三个能级,且每个能级上的电子数相等,核外电子排布为1s22s22p2,故Y为C元素;R与Y同一主族,结合原子序数可知,R为Si,而Z原子单电子数在同周期元素中最多,则外围电子排布为ns2np3,原子序数小于Si,故Z为N元素;W形成的单质是空气的主要成分之一,则W为O元素;Q的最外层只有一个电子,其他电子层电子均处于饱和状态,不可能为短周期元素,原子序数小于30,故核外电子排布为1s22s22p63s23p63d104s1,则Q为Cu元素,
(1)Cu+核外电子排布式为:1s22s22p63s23p63d10,故答案为:1s22s22p63s23p63d10;
(2)化合物CH4中C形成4个δ键,杂化方式为sp3,NO3-离子中N原子孤电子对数为$\frac{5+1-3×2}{2}$=0、价层电子对数为3,故其立体构型是平面三角形,
故答案为:sp3;平面三角形;
(3)Y、R的最高价氧化物分别为二氧化碳、二氧化硅,SiO2为原子晶体,CO2为分子晶体,故沸点较高的是 SiO2,
故答案为:SiO2; SiO2为原子晶体,CO2为分子晶体;
(4)Cu元素可形成一种化合物[Cu(NH3)4]SO4,为离子化合物,含有配位键、离子键和极性共价键,故答案为:配位键,极性共价键,离子键;
(5)碳有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为:4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8;
每个Y与周围的4个Y原子相邻,故Y原子的配位数为4;
若晶胞的边长为a pm,则晶胞体积为(a×10-10)3cm3,晶体的密度为ρ g/cm3,则晶胞质量为(a×10-10)3cm3×ρ g/cm3=ρa3×10-30ρ g,则8×$\frac{12}{{N}_{A}}$g=ρa3×10-30ρ g,故NA=$\frac{{96×{{10}^{30}}}}{{{a^3}•ρ}}$,
故答案为:8;4;$\frac{{96×{{10}^{30}}}}{{{a^3}•ρ}}$.
点评 本题是对物质结构的考查,为高考常见题型,侧重于学生的分析、计算能力的考查,涉及核外电子排布、杂化轨道、分子构型、晶体类型与性质、配合物、晶胞结构与计算等,需要学生具备扎实的基础,难度中等.

| A. | 溶质的质量分数为w=$\frac{a}{Vρ-a}$×100% | |
| B. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$ mol•L-1 | |
| C. | 上述溶液中再加入相同质量的水后,所得溶液的物质的量浓度变为原来一半 | |
| D. | 上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
| A. | 碳纳米管和C60都是单质 | |
| B. | 碳纳米管和金刚石的结构和性质相同 | |
| C. | 碳纳米管和石墨互为同素异形体 | |
| D. | 碳纳米管也能在空气中燃烧生成二氧化碳 |
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨(或光化学烟雾);
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”).
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
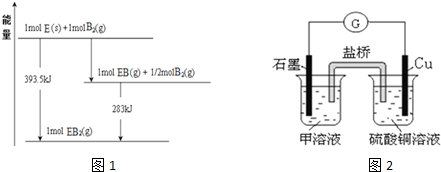
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液(或铁氰化钾溶液),若溶液紫色褪去(或产生蓝色沉淀),则产品中含有Fe2+.
(7)A与D形成的化合物分子中,各原子最外层均达8电子结构,则该分子的电子式为
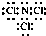 .
. | A. | 需要加热的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| D. | 伴随能量变化的物质变化都是化学变化 |
述中正确的是( )
| A. | 中性溶液AG=0 | |
| B. | 酸性溶液AG>0 | |
| C. | 常温下0.1mol/L的氢氧化钠溶液的AG=12 | |
| D. | 常温下0.1mol/L的醋酸溶液的AG=12 |
