题目内容
15.某元素的原子序数为33,写出该元素原子的核外电子排布式1S22S22P63S23P63d104S24P3,此元素的原子中被电子占据的轨道有18个,有8 个能级(能量不同的轨道).分析 根据核外电子排布规律可以写出33号元素的核外电子排布式为1S22S22P63S23P63d104S24P3,该元素原子中被电子占据的轨道,s轨道有4个,p轨道有9个,d轨道有5个,所以占据的轨道总共有18个,该原子电子占据的能级有1S、2S、2P、3S、3P、3d、4S、4P总共有8个,由此分析解答.
解答 解:根据核外电子排布规律可以写出33号元素的核外电子排布式为1S22S22P63S23P63d104S24P3,该元素原子中被电子占据的轨道,s轨道有4个,p轨道有9个,d轨道有5个,所以占据的轨道总共有18个,该原子电子占据的能级有1S、2S、2P、3S、3P、3d、4S、4P总共有8个,故答案为:1S22S22P63S23P63d104S24P3,18,8个.
点评 本题考查了原子核外电子排布规律,熟练掌握能量最低原理、泡利不相容原理、洪特规则是解答本题的关键,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
5.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于电解质的是BCD.
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.氯化钠
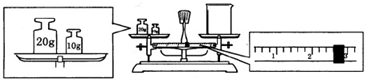
(2)某同学欲称量“鲜花保鲜剂”的质量,先用托盘天平称量烧杯的质量,天平平衡后的状态如图.则烧杯的实际质量为27.4g.
(3)配制上述一“鲜花保鲜剂”240mL所需的仪器有:烧杯、天平、药匙、量筒、玻璃棒、胶头滴管、250mL容量瓶.(在横线上填写所缺仪器的名称)
(4)容量瓶使用前必须进行的操作为检查是否漏水.
(5)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的最浓度为0.084mol/L:若检验“鲜花保鲜剂”溶液中的SO42-,你选择的化学试剂为BaCl2(填化学式).
(6)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是:④.
①没有洗涤烧杯和玻璃捧
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线.
| 成分 | 质量(g) | 摩尔质量(g.mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 3.48 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.32 | 158 |
| 氯化钠 | 0.08 | 58.5 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.氯化钠
(2)某同学欲称量“鲜花保鲜剂”的质量,先用托盘天平称量烧杯的质量,天平平衡后的状态如图.则烧杯的实际质量为27.4g.

(3)配制上述一“鲜花保鲜剂”240mL所需的仪器有:烧杯、天平、药匙、量筒、玻璃棒、胶头滴管、250mL容量瓶.(在横线上填写所缺仪器的名称)
(4)容量瓶使用前必须进行的操作为检查是否漏水.
(5)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的最浓度为0.084mol/L:若检验“鲜花保鲜剂”溶液中的SO42-,你选择的化学试剂为BaCl2(填化学式).
(6)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是:④.
①没有洗涤烧杯和玻璃捧
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线.
6.化学反应终点的判断是化学定量实验的重要环节.下列对化学反应终点的判断不正确的是( )
| A. | 向BaCl2溶液中加入足量Na2CO3溶液后,静置,向上层清澈中继续滴加Na2CO3溶液,若无沉淀,说明Ba2+已经完全沉淀 | |
| B. | 淀粉在稀硫酸的作用下水解后,加NaOH溶液使溶液呈碱性,加入新制Cu(OH)2,加热,若有砖红色沉淀生成,说明淀粉已经完全水解 | |
| C. | 将NaSO4•10H2O晶体置于坩埚内加热,称量,并重复上述操作,若相邻两次称量的结果相同,说明硫酸钠已全部失去结晶水 | |
| D. | 用酸式滴定管向滴有酚酞的NaOH溶液中滴加HCl溶液,若滴入最后一滴HCl溶液后红色刚好褪去,且30s内颜色不复原,说明NaOH已完全中和 |
20.取一定质量的Cu、Cu2O、CuO的固体混合物,将其分成两等份.其中一份通入足量的氢气充分反应后固体质量为25.6g,另一份加入500mL稀硝酸中固体恰好完全溶解并产生标准状况下的NO气体4.48L.已知Cu2O+2H+═Cu+Cu2++H2O.则稀硝酸的浓度为( )
| A. | 2 mol•L-1 | B. | 1.6 mol•L-1 | C. | 0.8 mol•L-1 | D. | 0.4 mol•L-1 |
4.现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应,但反应很快停止;
②B溶液与 C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出下列物质的名称:X二氧化碳.
(2)鉴别B在溶液中产生的阴离子的实验操作方法是取少量生B的溶液于试管,先加入盐酸,再加入BaCl2溶液,生成白色沉淀,则溶液中含有SO42-.
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:CO32-+2H+=CO2↑+H2O
B与C反应至溶液呈中性:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓
(4)D 与E的混合物ag,加入足量盐酸,反应完毕生成标准状况时的气体 bL,则D在混合物中的质量分数为$\frac{(22.4a-197b)}{22.4a}$×100%.
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应,但反应很快停止;
②B溶液与 C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出下列物质的名称:X二氧化碳.
(2)鉴别B在溶液中产生的阴离子的实验操作方法是取少量生B的溶液于试管,先加入盐酸,再加入BaCl2溶液,生成白色沉淀,则溶液中含有SO42-.
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:CO32-+2H+=CO2↑+H2O
B与C反应至溶液呈中性:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓
(4)D 与E的混合物ag,加入足量盐酸,反应完毕生成标准状况时的气体 bL,则D在混合物中的质量分数为$\frac{(22.4a-197b)}{22.4a}$×100%.
5.如图是部分短周期元素原子半径与原子序数的关系图.下列说法正确的是( )
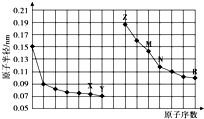

| A. | 最高价氧化物对应水化物的碱性:Z<M | |
| B. | Y、R两种元素气态氢化物的沸点:Y<R | |
| C. | X、N两种元素组成的化合物不与任何酸反应 | |
| D. | 简单离子的半径:Z<X<R |
 ;
; ;
; .
. .
.