题目内容
7.草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,分解方程式为:H2C2O4$\stackrel{加热}{→}$H2O+CO2↑+CO↑.请按要求完成下列实验(可选用下列装置,要求操作简单,现象明显,保证安全).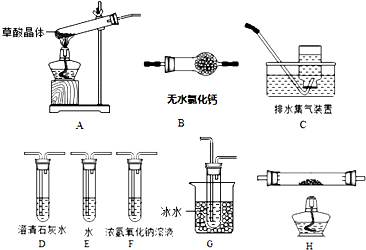
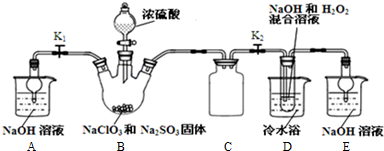
(1)通过实验证明草酸晶体的分解产物中含有CO2,选用的装置有AGDC,证明有CO2生成的实验现象是D有气泡冒出,澄清石灰水变浑浊.如果选用装置G其主要作用是冷凝分解产物中的草酸,防止干扰CO2的检验(不选G不用作答).
(2)①证明草酸晶体的分解产物中含有CO,要求看到至少两个明显现象,实验中选用的装置的合理连接顺序为A、F、D、B、H、D、C(装置可重复使用).装置H反应管中盛有的物质是CuO.②能证明草酸晶体的分解产物中含有CO的现象H中黑色粉末变为红色,其后的D中澄清石灰水变浑浊.
(3)已知:碳酸电离常数为:K1=4.4×l0-7,K2=4.7×l0-11.写出Na2CO3溶液中滴加少量草酸溶液的离子方程式2CO32-+H2C2O4=C2O42-+2HCO3-.
分析 (1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳而使澄清石灰水变浑浊;草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,G装置温度较低,有冷凝作用,防止干扰实验;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用碱石灰干燥CO,利用CO的还原性将CO氧化,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO;H装置中盛放的物质应该具有氧化性,且和CO反应有明显现象发生;
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊;
(3)由K可知酸性强弱,发生强酸制取弱酸的反应.
解答 解:(1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳,二氧化碳和氢氧化钙反应生成难溶性的碳酸钙沉淀而使澄清石灰水变浑浊,所以C中观察到的现象是:有气泡冒出且澄清石灰水变浑浊,说明有二氧化碳生成,则证明草酸晶体的分解产物中含有CO2,选用的装置有AGDC;
草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,草酸易挥发,导致生成的气体中含有草酸,草酸和氢氧化钙反应生成难溶性的草酸钙而干扰二氧化碳的检验,G装置温度较低,有冷凝作用,防止干扰二氧化碳的检验,
故答案为:AGDC;D有气泡冒出,澄清石灰水变浑浊;冷凝(水蒸气和草酸),防止草酸进入装置C反应生成沉淀而干扰CO2的检验;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用碱石灰干燥CO,利用CO和CuO发生还原反应生成CO2,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO避免环境污染,所以其连接顺序是A、F、D、B、H、D、C;
H装置中盛放的物质应该具有氧化性,且和CO反应有明显现象发生,CuO能被CO还原且反应过程中黑色固体变为红色,现象明显,所以H中盛放的物质是CuO,
故答案为:A、F、D、B、H、D、C;CuO;
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊,且CO将黑色的CuO还原为红色的Cu,只要H中黑色固体转化为红色且其后的D装置溶液变浑浊就说明含有CO,
故答案为:H中黑色粉末变为红色,其后的D中澄清石灰水变浑浊;
(3)由K可知酸性强弱,则Na2CO3溶液中滴加少量草酸溶液的离子方程式为2CO32-+H2C2O4=C2O42-+2HCO3-,故答案为:2CO32-+H2C2O4=C2O42-+2HCO3-.
点评 本题考查物质制备实验和性质实验方案设计,为高频考点,侧重考查学生知识综合应用、实验基本操作能力及实验方案设计能力,综合性较强,难点是排列实验先后顺序,根据实验目的及物质的性质进行排列顺序,注意要排除其它因素干扰,题目难度较大.

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案| A. | 过滤操作时,为了过滤效果好,要用玻璃棒搅拌 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,为了防止局部过热,要用玻璃棒搅拌 |
| A. | Na2O2是碱性氧化物 | |
| B. | Na2O2中阴阳离子个数比为1:1 | |
| C. | 可用澄清石灰水来区分Na2CO3 和NaHCO3 | |
| D. | 与同浓度盐酸反应的剧烈程度:NaHCO3>Na2CO3 |

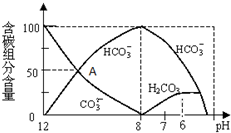
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节PH,除去溶液中Al3+(使溶液中Al3+生成氢氧化物沉淀),该工艺中“搅拌”的作用是使反应物充分接触,加快反应速率,使反应充分进行.
(2)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是防止蒸发时温度过高,碱式硫酸铁进一步水解生成Fe(OH)3.
(3)反应Ⅱ中的离子方程式为Fe2++2H++NO2-=Fe3++NO↑+H2O或Fe2++H2O+NO2-=Fe(OH)2++NO↑+H+,在实际生产中,反应Ⅱ常同时通入O2循环使用产物以减少NaNO2的用量,O2的作用是2H2O+4NO+O2=4HNO3(或2NO+O2=2NO23NO2+H2O=2HNO3+NO).(用化学方程式表示)
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.(填写字母)
A.溴水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.
(1)D元素基态原子的电子排布式为1s22s22p63s23p63d104s24p3或[Ar]3d104s24p3.
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为P>S>Si(用相应的元素符号作答).
(3)B、X、D氢化物的沸点由高到低的顺序为NH3>AsH3>PH3(用相应的化学式作答).
(4)E元素是A元素所在周期中电负性最大的,试推测下列微粒的立体构型:
| 微粒 | EO2- | EO3- |
| 立体构型名称 |
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
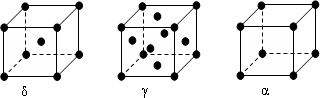
(6)F元素基态原子M层上有5对成对电子,请解释F晶体能导电的原因铁是金属晶体,由金属阳离子和自由电子组成,自由电子在外加电场的作用下可发生定向移动,因此铁能导电.F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为4:6:3,δ、γ、α三种晶胞的边长之比为$\frac{2}{\sqrt{3}}$:$\sqrt{2}$:1.