题目内容
 (1)反应A+3B=2C+2D在四种不同情况下的反应速率分别为
(1)反应A+3B=2C+2D在四种不同情况下的反应速率分别为①v(A)=0.15mol/(L.min)
②v(B)=0.6mol/(L.min)
③v(C)=0.4mol/(L.min)
④v(D)=0.01mol/(L.s )
该反应进行的快慢顺序为
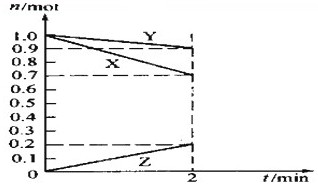
(2)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化如图所示.则该反应的化学方程式为
考点:物质的量或浓度随时间的变化曲线,化学反应速率和化学计量数的关系
专题:化学平衡专题,化学反应速率专题
分析:(1)根据化学反应速率之比等于方程式的系数之比,将用不同物质表示的化学反应速率统一用同一种物质来表示,然后再进行数据的大小比较即可;
(2)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;根据v=
计算反应速率.
(2)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;根据v=
| △c |
| △t |
解答:
解:(1)把所有速率都换算成v(A),根据同一反应,速率之比等于计量数之比.
①v(A)=0.15mol/(L.min)
②当v(B)=0.6mol/(L?min)时,v(A)=0.2mol/(L?min);
③当v(C)=0.4 mol/(L?min)时,v(A)=0.2mol/(L?min);
④当v(D)=0.01mol/(L?s)时,v(A)=0.005 mol/(L?s)=0.30mol/(L?min);
所以该反应进行的快慢顺序为④>②=③>①;
故答案为:④>②=③>①;
(2)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y 2Z;
2Z;
v(Z)=
=
=0.05mol?(L?min)-1,
故答案为:3X+Y 2Z;0.05mol?(L?min)-1.
2Z;0.05mol?(L?min)-1.
①v(A)=0.15mol/(L.min)
②当v(B)=0.6mol/(L?min)时,v(A)=0.2mol/(L?min);
③当v(C)=0.4 mol/(L?min)时,v(A)=0.2mol/(L?min);
④当v(D)=0.01mol/(L?s)时,v(A)=0.005 mol/(L?s)=0.30mol/(L?min);
所以该反应进行的快慢顺序为④>②=③>①;
故答案为:④>②=③>①;
(2)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y
 2Z;
2Z;v(Z)=
| △c |
| △t |
| ||
| 2min |
故答案为:3X+Y
 2Z;0.05mol?(L?min)-1.
2Z;0.05mol?(L?min)-1.
点评:本题考查了反应速率的计算、化学平衡图象分析,题目难度中等,注意分析各物质的量的变化曲线,把握化学方程式的判断方法.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
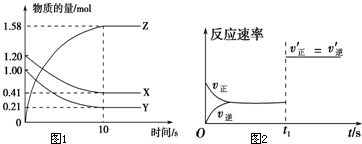 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图1所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图1所示: 和
和
 和
和

 A、B、C、D、E各物质的转化关系如图所示.
A、B、C、D、E各物质的转化关系如图所示. 某同学设计出如下装置成功的证明了Cu和Ag的金属活动性顺序.请你原电池原理和实验装置,完成下列实验报告.
某同学设计出如下装置成功的证明了Cu和Ag的金属活动性顺序.请你原电池原理和实验装置,完成下列实验报告.