题目内容
4.下列溶液中各微粒的浓度关系正确的是( )| A. | 0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1 | |
| B. | 0.1 mol/L NaHCO3溶液中,c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 0.1 mol/L 的NaHA溶液,其pH=4,则c(HA-)>c(A2-)>c(H2A) | |
| D. | 只含Na+、CH3COO-、H+、OH-的酸性溶液中,c(H+)>c(CH3COO-)>c(Na+)>c(OH-) |
分析 A.醋酸浓度越大,醋酸的电离程度越小,则前、后醋酸溶液中氢离子浓度之比小于2:1;
B.根据碳酸氢钠溶液中的物料守恒判断;
C.溶液呈酸性,则c(H+)>c(OH-),说明HA-的电离程度大于其水解程度,则c(A2-)>c(H2A);
D.c(H+)>c(CH3COO-)>c(Na+)>c(OH-)违反的电荷守恒.
解答 解:A.0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中,前者醋酸浓度较大,醋酸的电离程度较小,则前后溶液中c(H+)之比小于2:1,故A错误;
B.0.1 mol/L NaHCO3溶液中,根据物料守恒可得:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),故B错误;
C.0.1 mol/L 的NaHA溶液的pH=4,说明HA-的电离程度大于其水解程度,则c(A2-)>c(H2A),溶液中离子浓度大小为:c(HA-)>c(A2-)>c(H2A),故C正确;
D.只含Na+、CH3COO-、H+、OH-的酸性溶液中:c(H+)>c(OH-),根据核电荷数可知:c(CH3COO-)>c(Na+),该溶液应该醋酸钠与醋酸的混合液,则c(CH3COO-)>c(H+),溶液中正确的离子浓度大小可能为:c(CH3COO-)>c(H+)>c(Na+)>c(OH-)或c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故D错误;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.化工生产需要用到各种原料,其中与事实相符合的是( )
| A. | 用乙醇和浓硫酸制乙烯 | B. | 用电解水获得的氢气来合成氨 | ||
| C. | 用晒盐后的卤水制溴单质 | D. | 用氢氧化钠和二氧化碳制碳酸钠 |
15.在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH(aq)}{→}$Fe(OH)2 | |
| B. | Al3+$\stackrel{过量氨水}{→}$Al${\;}_{2}^{-}$$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| C. | NH3$\stackrel{O_{2}}{→}$NO$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | 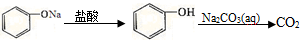 |
12.氢气、甲烷完全燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
将氢气、甲烷按一定比例混合,所得气体的密度是相同条件下N2的$\frac{1}{2}$,则9.8g该混合物完全燃烧能放出的热量最多为( )
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
将氢气、甲烷按一定比例混合,所得气体的密度是相同条件下N2的$\frac{1}{2}$,则9.8g该混合物完全燃烧能放出的热量最多为( )
| A. | 280.58kJ | B. | 562.76kJ | C. | 530.58kJ | D. | 890.3kJ |
19.今年“世界水日”主题“关注水质、抓住机遇、应对挑战”,下列与主题不符的是( )
| A. | 上海属“水质性缺水”,保护水资源刻不容缓 | |
| B. | 提倡节水产业,加强废水处理 | |
| C. | 只喝桶装水或功能性饮料以保证饮用水质量 | |
| D. | 用再生水灌溉城市绿地 |
9.组成生命细胞的11种宏量元素(约占人体总质量的99.97%),全部位于周期表的前20号.其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素.
(1)这六种元素中除H、C、O、P、S外,应该还有N(写元素符号),它的原子最外层共有5种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置第二周期IVA族.
(2)糖类是人体获得能量的来源之一.已知1mol 葡萄糖在人体内完全氧化为二氧化碳和水,放出2804kJ的热量,该反应的热化学方程式C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804kJ•mol-1.
(3)CO2是一种温室气体,它的电子式为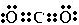 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
(4)元素周期表中元素的性质存在递变规律,下列关系正确的是d(填序号).
a.离子半径:S2->Na+>O2->H+ b.与水反应的剧烈程度:K>Na>Mg>Ca
c.熔点:CO2>SiO2>Na2O>SO3 d.还原性:PH3>H2S>HCl>HF
(5)表为部分非金属元素与氢形成共价键的键长与键能数据:
根据表中数据,归纳共价键键能与键长的关系同类分子中(同主族元素原子与相同其他原子等合理均可),键长越小,键能越大.
(1)这六种元素中除H、C、O、P、S外,应该还有N(写元素符号),它的原子最外层共有5种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置第二周期IVA族.
(2)糖类是人体获得能量的来源之一.已知1mol 葡萄糖在人体内完全氧化为二氧化碳和水,放出2804kJ的热量,该反应的热化学方程式C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804kJ•mol-1.
(3)CO2是一种温室气体,它的电子式为
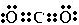 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.(4)元素周期表中元素的性质存在递变规律,下列关系正确的是d(填序号).
a.离子半径:S2->Na+>O2->H+ b.与水反应的剧烈程度:K>Na>Mg>Ca
c.熔点:CO2>SiO2>Na2O>SO3 d.还原性:PH3>H2S>HCl>HF
(5)表为部分非金属元素与氢形成共价键的键长与键能数据:
| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
16.下列说法正确的是( )
| A. | 难失去电子的原子,易形成阴离子 | |
| B. | 只有化合物分子中才存在共价键 | |
| C. | 共价分子中所有原子都具有8电子稳定结构 | |
| D. | 含氧酸的组成中可以含有金属元素 |
 .
.