��Ŀ����
17��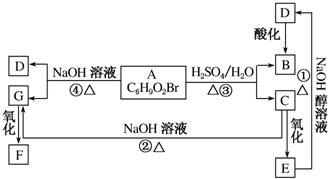 �л���A��B��C��D��E��F��G���ϵ��ͼ��ʾ����֪F�����к���������ͬ�Ĺ����ţ�5.2gF����100mL1mol•L-1��NaOH��Һǡ����ȫ�кͣ�D�ķ���ʽΪC3H3O2Na��E�ķ����к����Ȼ���
�л���A��B��C��D��E��F��G���ϵ��ͼ��ʾ����֪F�����к���������ͬ�Ĺ����ţ�5.2gF����100mL1mol•L-1��NaOH��Һǡ����ȫ�кͣ�D�ķ���ʽΪC3H3O2Na��E�ķ����к����Ȼ�����1��ָ����ѧ��Ӧ���ͣ�����ȥ��Ӧ����ȡ����ˮ�ⷴӦ��
��2��д���������ʵĽṹ��ʽ��DCH2�TCH-COONa��FHOOC-CH2-COOH��
��3��д����Ӧ�۵Ļ�ѧ����ʽCH2�TCH-COOCH2CH2CH2Br+H2O$��_{��}^{H_{2}SO_{4}}$CH2�TCH-COOH+BrCH2CH2CH2OH��
���� A�в����Ͷ�=$\frac{6��2+2-10}{2}$=2��A�ܷ���ˮ�ⷴӦ˵�����������������䲻���Ͷ�֪��A�л�����̼̼˫����Aˮ������B��C��C�ܷ���������Ӧ����C�к��д��ǻ���BΪ���ᣬC����һϵ�з�Ӧ������B����B��C��̼ԭ�Ӹ������Ϊ3��E�ܺ��������ƵĴ���Һ������ȥ��Ӧ����C��E�к���-Br��D�ữ�õ�B������B��D�к���̼̼˫������BΪCH2=CHCOOH��DΪCH2=CHCOONa��A���������Ƶ�ˮ��Һ����ˮ�ⷴӦ����D��G��G�ܷ���������Ӧ����F��GΪ�����Һ����������ǻ��������ʽΪC3H8O2��F�ܺ�NaOH��Һ��Ӧ��FΪ���ᣬ���F�Ƕ�Ԫ���ᣬ�к�0.1molNaOH��ҪF0.05mol������Ϊ0.05mol��104g•mol-1=5.2g������FΪ��Ԫ���ᣬ��F�ṹ��ʽΪHOOCCH2COOH��G�ṹ��ʽΪHOCH2CH2COOH��CΪBrCH2CH2CH2OH��EΪBrCH2CH2COOH��AΪCH2=CHCOOCH2CH2CH2Br���˷������
��� �⣺A�в����Ͷ�=$\frac{6��2+2-10}{2}$=2��A�ܷ���ˮ�ⷴӦ˵�����������������䲻���Ͷ�֪��A�л�����̼̼˫����Aˮ������B��C��C�ܷ���������Ӧ����C�к��д��ǻ���BΪ���ᣬC����һϵ�з�Ӧ������B����B��C��̼ԭ�Ӹ������Ϊ3��E�ܺ��������ƵĴ���Һ������ȥ��Ӧ����C��E�к���-Br��D�ữ�õ�B������B��D�к���̼̼˫������BΪCH2=CHCOOH��DΪCH2=CHCOONa��A���������Ƶ�ˮ��Һ����ˮ�ⷴӦ����D��G��G�ܷ���������Ӧ����F��GΪ�����Һ����������ǻ��������ʽΪC3H8O2��F�ܺ�NaOH��Һ��Ӧ��FΪ���ᣬ���F�Ƕ�Ԫ���ᣬ�к�0.1molNaOH��ҪF0.05mol������Ϊ0.05mol��104g•mol-1=5.2g������FΪ��Ԫ���ᣬ��F�ṹ��ʽΪHOOCCH2COOH��G�ṹ��ʽΪHOCH2CH2COOH��CΪBrCH2CH2CH2OH��EΪBrCH2CH2COOH��AΪCH2=CHCOOCH2CH2CH2Br��
��1��ͨ�����Ϸ���֪���٢ֱܷ�����ȥ��Ӧ��ȡ����ˮ�ⷴӦ��
�ʴ�Ϊ����ȥ��Ӧ��ȡ����ˮ�⣩��Ӧ��
��2��ͨ�����Ϸ���֪��D��F�ṹ��ʽ�ֱ���CH2�TCH-COONa��HOOC-CH2-COOH���ʴ�Ϊ��CH2�TCH-COONa��HOOC-CH2-COOH��
��3��AΪCH2=CHCOOCH2CH2CH2Br��Aˮ�����ɱ�ϩ���3-��-1-������ˮ�ⷽ��ʽΪCH2�TCH-COOCH2CH2CH2Br+H2O$��_{��}^{H_{2}SO_{4}}$CH2�TCH-COOH+BrCH2CH2CH2OH��
�ʴ�Ϊ��CH2�TCH-COOCH2CH2CH2Br+H2O$��_{��}^{H_{2}SO_{4}}$CH2�TCH-COOH+BrCH2CH2CH2OH��
���� ���⿼���л����ƶϣ����ؿ���ѧ�������ж��������漰±�������������ᡢϩ��֮���ת������ȷ�ж���ԭ��λ���ǽⱾ��ؼ���ע���л������ȥ��Ӧʱ�ṹ�ص㣬��Ŀ�ѶȲ���

 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�| A�� | ���ʵ���Ũ����ȵ�CH3COOH��CH3COONa��Һ�������Ϻ����Һ�У�2 c ��Na+��=c��CH3COO-��+c��CH3COOH�� | |
| B�� | ��0.4mol/LNH4Cl��Һ��0.2mol/LNaOH��Һ�������Ϻ���Һ�����ӵ����ʵ���Ũ�ȴ�С��ϵΪ��c��NH4+����c��Na+����c��NH3•H2O����c��OH-����c��H+�� | |
| C�� | ����ˮ�������ϸ��¶ȣ�ˮ�����ӻ����pH������� | |
| D�� | ��ϡ��ˮ��ˮϡ�ͣ�$\frac{c��N{H}_{4}^{+}��}{c��N{H}_{3}��{H}_{2}O��}$ ���� |
| A�� | ����ԭ�ӻ���ԭ��֮�������ýл�ѧ�� | |
| B�� | ���������Ӽ�ͨ�������������γɵĻ�ѧ���������Ӽ� | |
| C�� | ֻ�н���Ԫ�غͷǽ���Ԫ�ػ���ʱ�����γ����Ӽ� | |
| D�� | ���ӻ�������һ���������Ӽ� |
| A�� | �ӳ�-��ȥ-ˮ�� | B�� | ��ȥ-ˮ��-�ӳ� | C�� | ��ȥ-�ӳ�-ˮ�� | D�� | ȡ��-��ȥ-�ӳ� |
| A�� | ��x��4ʱ����Ϊ���壨���³�ѹ�£� | |
| B�� | yһ����ż�� | |
| C�� | �ֱ�ȼ��1mol����������x+$\frac{y}{4}$��mol | |
| D�� | ��150��ʱ���ܱ���������ȫȼ�պ�ָ���ԭ�¶ȣ���õ�ѹǿһ����ȼ��ǰ���� |
| A�� | N2 | B�� | F2 | C�� | O2 | D�� | C12 |
��1����������Ӧ��ʵ���У����ᡢ�Ҵ���������ƽ��ʱ�������������������±����ɱ��������Ʋ⣬��ֵx�ķ�Χ��1.57��x��1.76��
| ��Ӧ | �Ҵ���mol�� | ���ᣨmol�� | ����������mol�� |
| 1 | 2 | 2 | 1.33 |
| 2 | 3 | 2 | 1.57 |
| 3 | 4 | 2 | x |
| 4 | 5 | 2 | 1.76 |
����������м������������ƹ��壬��ʱ��Һ��$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$����С���������С�����䡱����
����������м���ϡNaOH��Һ��ʹ��ǡ����ȫ��Ӧ��������Һ��pH��7���������������=�����������ӷ���ʽ������ԭ��CH3COO-+H2O?CH3COOH+OH-��
����������м���pH=11��NaOH��Һ���Ҷ��ߵ������Ϊ1��1����������Һ�и����ӵ����ʵ���Ũ���ɴ�С��˳����c��CH3COO-����c��Na+����c��H+����c��OH-����
�ܵ������Ũ��Ϊ0.1mol/Lʱ����ʱ����ĵ��볣��ԼΪ1��10-5��
| A�� | NH4HCO3������ķ�Ӧ�Ƿ��ȷ�Ӧ | |
| B�� | �÷�Ӧ�У�����ת��Ϊ�����ڲ������� | |
| C�� | ��Ӧ�������������������������� | |
| D�� | ���Ѿɻ�ѧ�����յ�������С���γ��»�ѧ���ų��������� |
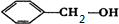 ��
��