题目内容
8.下列说法中正确的是( )| A. | 两个原子或多个原子之间的相互作用叫化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中一定含有离子键 |
分析 A.相邻原子之间的强烈的相互作用为化学键;
B.阴、阳离子间通过静电作用而形成的化学键叫做离子键;
C.铵盐为离子化合物,含有离子键;
D.离子键只存在离子化合物中.
解答 解:A.原子之间的作用力不一定为化学键,只有相邻原子之间的强烈的相互作用为化学键,故A错误;
B.阴、阳离子间通过静电作用而形成的化学键叫做离子键,包括静电吸引和静电排斥,故B错误;
C.铵盐为离子化合物,含有离子键,但为非金属元素形成的化合物,故C错误;
D.离子键只存在离子化合物中,则离子化合物中一定含有离子键,故D正确.
故选D.
点评 本题考查共价键知识,为高频考点,侧重于学生的分析能力和基本概念知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列各对物质中,互为同分异构体的是( )
| A. | CH3CH2CH2CH3和CH3CH=CHCH3 | B. | CH3CH=CHCH3和 CH3C≡CCH3 | ||
| C. | CH3CH=CHCH3和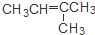 | D. | CH3CH2CH2OH和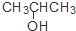 |
16.下列关于物质用途的说法正确的是( )
| A. | SO2可用来漂白馒头、银耳等食品 | |
| B. | 纯净的二氧化硅是制备光导纤维的原料 | |
| C. | 氢氧化铝可以用做耐火材料 | |
| D. | 四氧化三铁常用作红色油漆和涂料 |
3.用水稀释0.1mol•L-1氨水时,溶液中随水量的增加而减小的是( )
| A. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | C. | n(OH-)和c(H+) | D. | c(H+)和c(OH-)的乘积 |
13.同周期的X、Y、Z三种元素的最高价氧化物对应水化物分别是:H3XO4、H2YO4、HZO4,下列判断正确的是( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
⑤酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4.
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
⑤酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4.
| A. | ①② | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②③④ |
20.下列说法正确的是( )
| A. |  如图可表示水分解过程中的能量变化 如图可表示水分解过程中的能量变化 | |
| B. | 若2C(s)+O2(g)=2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol | |
| C. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| D. | 已知:Ⅰ:对于反应:H2(g)+Cl2(s)=2HCl (g)△H=-a kJ/mol, Ⅱ: 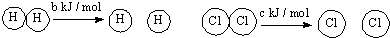 且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为-a-b-c 且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为-a-b-c |
18.下列说法不正确的是( )
| A. | 等质量的乙醛和乙酸乙酯完全燃烧时消耗氧气的量不相等 | |
| B. | 淀粉水解的最终产物在加热条件下可与新制氢氧化铜反应生成砖红色沉淀 | |
| C. | 可用饱和碳酸钠溶液除去乙酸乙酯中的乙酸 | |
| D. | 2-氯-2-甲基丙烷在氢氧化钠的醇溶液中加热可生成甲基丙烯 |
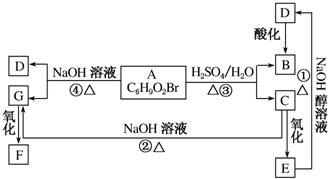 有机物A、B、C、D、E、F、G相互关系如图所示.已知F分子中含有两个相同的官能团,5.2gF能与100mL1mol•L-1的NaOH溶液恰好完全中和.D的分子式为C3H3O2Na,E的分子中含有羧基.
有机物A、B、C、D、E、F、G相互关系如图所示.已知F分子中含有两个相同的官能团,5.2gF能与100mL1mol•L-1的NaOH溶液恰好完全中和.D的分子式为C3H3O2Na,E的分子中含有羧基.