题目内容
4. 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
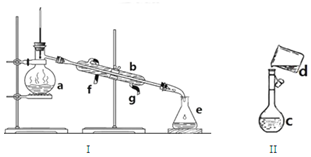
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.(1)写出下列仪器的名称:b.冷凝器(管)、c.容量瓶
(2)若用装置I分离水和酒精的混合物,还缺少的仪器是酒精灯,将仪器补充完整后进行实验,温度计水银球的位置在蒸馏烧瓶支管口处处.冷凝水由g口通入,f口流出(填f或g)
(3)现需配制0.1mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图.
①图中的错误是没有用玻璃棒引流
②根据计算得知,所需NaOH的质量是2.0g.
分析 (1)根据仪器的结构特点判断;
(2)用装置I分离水和酒精的混合物,为蒸馏操作;蒸馏时,温度计用于测量馏分的温度,冷凝水由下口通入、上口流出;
(3)配制溶液时需用玻璃棒引流,且用500mL的容量瓶.
解答 解:(1)由仪器的图形可知b为冷凝器(管),c为容量瓶,故答案为:冷凝器(管);容量瓶;
(2)用装置I分离水和酒精的混合物,为蒸馏操作,还需要酒精灯,且蒸馏时,温度计用于测量馏分的温度,位于蒸馏烧瓶支管口处,冷凝水由下口通入、上口流出,以充满冷凝管,达到充分冷凝的目的,
故答案为:酒精灯;蒸馏烧瓶支管口处; g;f;
(3)①配制溶液时需用玻璃棒引流,缺少玻璃棒,故答案为:没有用玻璃棒引流;
②应用500mL的容量瓶,则m(NaOH)=nM=0.5L×0.1mol/L×40g/mol=2.0 g,故答案为:2.0 g.
点评 本题考查混合物分离提纯方法的选择和应用以及溶液的配制,为高频考点,把握物质的性质及性质的差异为解答的关键,侧重混合物分离方法的考查,把握配制溶液的方法,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
10.2015年 10月,中国科学家屠呦呦获得了诺贝尔生理学奖,获奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.青蒿素的分子式为 C15H22O5,则关于青蒿素的说法中正确的是( )
| A. | 青蒿素是一种氧化物 | |
| B. | 青蒿素的摩尔质量为 282 | |
| C. | 56.4g青蒿素中所含氧原子数目为 6.02×1023个 | |
| D. | 青蒿素中 C、H、O元素的质量比为 15:22:5 |
12.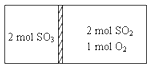 一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g)H=196kJ•moL现有密闭容器,中间隔板不能传导热量但可自由滑动,按如图所示投料,一段时间达到平衡时,下列说法正确的( )
一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g)H=196kJ•moL现有密闭容器,中间隔板不能传导热量但可自由滑动,按如图所示投料,一段时间达到平衡时,下列说法正确的( )
 一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g)H=196kJ•moL现有密闭容器,中间隔板不能传导热量但可自由滑动,按如图所示投料,一段时间达到平衡时,下列说法正确的( )
一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g)H=196kJ•moL现有密闭容器,中间隔板不能传导热量但可自由滑动,按如图所示投料,一段时间达到平衡时,下列说法正确的( )| A. | 恒温条件下,达到平衡容器两边SO3的体积分数相同 | |
| B. | 恒温条件下,容器中两边的吸收或放出的热量数值之和小于为196kJ | |
| C. | 若容器为绝热,达到平衡时右室反应速率等于左室反应速率 | |
| D. | 若容器为绝热容器,右室中SO2的转化率与左室SO3的转化率之和小于1 |
16.下列有关气体摩尔体积的说法中正确的是( )
| A. | 在标准状况下,1 mol任何物质的体积都约为22.4 L | |
| B. | 在标准状况下,0.5 mol任何气体的体积都约为11.2 L | |
| C. | 在常温常压下,1 mol任何气体的体积都约为22.4 L | |
| D. | 在标准状况下,0.5 mol CCl4所占有的体积约为11.2 L |
13.铅的冶炼大致过程如下:①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2$\frac{\underline{\;高温\;}}{\;}$2PbO+2SO2;③制粗铅:PbO+C$\frac{\underline{\;高温\;}}{\;}$Pb+CO;PbO+CO$\frac{\underline{\;高温\;}}{\;}$Pb+CO2.下列说法正确的是( )
| A. | 将1 mol PbS冶炼成Pb理论上至少需要6 g碳 | |
| B. | 浮选法富集方铅矿的过程属于化学变化 | |
| C. | 方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO | |
| D. | 整个冶炼过程中,制取1 mol Pb共转移2 mol电子 |
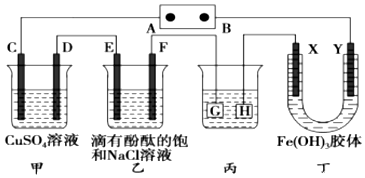
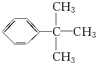 ;乙能被高锰酸钾酸性溶液氧化为分子式C8H6O4的羧酸,则乙可能的结构有9种.
;乙能被高锰酸钾酸性溶液氧化为分子式C8H6O4的羧酸,则乙可能的结构有9种. .
.