题目内容
16.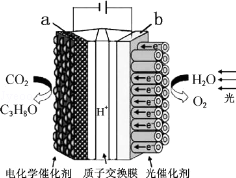 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )| A. | 该装置将化学能转化为光能和电能 | |
| B. | 该装置工作时,H+从a极区向b极区迁移 | |
| C. | 每生成3mol O2,有88gCO2被还原 | |
| D. | a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O |
分析 A.电解池是将电能转化为化学能的装置;
B.电解池工作时,电解质溶液中阳离子向阴极移动;
C.根据转移电子相等计算被还原二氧化碳质量;
D.a电极是阴极,阴极上二氧化碳得电子和氢离子反应生成C3H8O和水.
解答 解:A.电解池是将电能转化为化学能的装置,该装置有外接电源,所以是电解池,是将化学能转化为电能的装置,故A错误;
B.电解池工作时,电解质溶液中阳离子向阴极移动,所以该装置工作时,H+从b极区向a极区迁移,故B错误;
C.根据转移电子相等得被还原m(CO2)=$\frac{3mol×4}{6}×44g/mol$=88g,故C正确;
D.a电极是阴极,阴极上二氧化碳得电子和氢离子反应生成C3H8O和水,电极反应式为3CO2+18H++18e-=C3H8O+5H2O,故D错误;
故选C.
点评 本题考查电解原理,为高频考点,侧重考查基本概念、基本计算,难点是电极反应式的书写,易错点是离子移动方向判断,题目难度不大.

练习册系列答案
相关题目
7.下列实验操作或根据实验得出的结论正确的是( )
| A. | 镀锌层破损后即对镀锌铁(白铁)制品失去保护作用 | |
| B. | 制备氢氧化铁胶体时,应向FeCl3溶液中滴加NaOH溶液,并继续煮沸至液体呈红褐色 | |
| C. | 用托盘天平称取5.85g NaCl,称量时砝码放在右盘,氯化钠放在左盘 | |
| D. | 用灼烧闻气味的方法可以区别棉花和羊毛 |
11.下列反应的离子方程式正确的是( )
| A. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O | |
| B. | 稀盐酸除铁锈:6H++Fe2O3=2Fe3++3H2O | |
| C. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
1.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2.7g金属铝变成铝离子时失去的电子数目为0.2NA | |
| B. | 16g CH4与18 g NH4+ 所含质子数相等 | |
| C. | 标准状况下,22.4 L汽油所含的分子数为NA | |
| D. | 在0℃,1.01×105Pa时,11.2L氮气所含的原子数目为NA |
8.下列说法正确的是(NA表示阿伏加德罗常数)( )
| A. | 0.5 mol O3的质量为16 g | B. | 32 g O2中含有的氧分子数为2NA | ||
| C. | 1 g H2中含有电子数为1NA | D. | 3.01×1023个铜原子的质量为64 g |
19..煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数随温度的变化如下表:
试回答下列问题:
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有BCE(选填A、B、C、D、E);
(2)在1L密闭容器中通入10mol CO和10mol水蒸气,在500℃下经过30s达到平衡,则30s内CO的平均反应速率为0.25mol•L-1•s-1;
(3)已知在一定温度下,C(s)+CO2(g)?2CO(g)平衡常数K;K的表达式$\frac{{c}^{2}(CO)}{c(C{O}_{2})}$;
C(s)+H2O(g)?CO(g)+H2(g)平衡常数K1;CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是:K=$\frac{{K}_{1}}{{K}_{2}}$;
(4)某温度下C(s)+CO2(g)?2CO(g)能判断该反应达到化学平衡状态的依据是CEF;
A.c(CO2)=c(CO) B.K不变 C.容器中的压强不变
D.v正(CO)=2v正(CO2) E.c(CO)保持不变 F.混合气体相对分子质量不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g)?2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.

已知:CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有BCE(选填A、B、C、D、E);
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
(3)已知在一定温度下,C(s)+CO2(g)?2CO(g)平衡常数K;K的表达式$\frac{{c}^{2}(CO)}{c(C{O}_{2})}$;
C(s)+H2O(g)?CO(g)+H2(g)平衡常数K1;CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是:K=$\frac{{K}_{1}}{{K}_{2}}$;
(4)某温度下C(s)+CO2(g)?2CO(g)能判断该反应达到化学平衡状态的依据是CEF;
A.c(CO2)=c(CO) B.K不变 C.容器中的压强不变
D.v正(CO)=2v正(CO2) E.c(CO)保持不变 F.混合气体相对分子质量不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g)?2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.


 .
. .
. .
.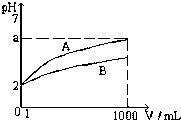 T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示
T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示