题目内容
10.在常温下发生下列反应:①16H++10Z-+2XO4-═2X2++5Z2+8H2O
②2A2++B2═2A3++2B-
③2B-+Z2═B2+2Z-
根据上述反应,判断下列结论中错误的是( )
| A. | 溶液中可能发生反应Z2+2A2+=2A3++2Z- | |
| B. | Z2在①③反应中作还原剂 | |
| C. | 氧化性强弱顺序为XO4->Z2>B2>A3+ | |
| D. | X2+是XO4-的还原产物 |
分析 ①16H++10Z-+2XO4-═2X2++5Z2+8H2O中,Z元素的化合价升高,X元素的化合价降低;
②2A2++B2═2A3++2B-中,A元素的化合价升高,B元素的化合价降低;
③2B-+Z2═B2+2Z-中,B元素的化合价升高,Z元素的化合价降低,则
A.若发生反应Z2+2A2+=2A3++2Z-,氧化性Z2>A3+,与②③中结论一致;
B.①中Z元素的化合价升高,③中Z元素的化合价降低;
C.氧化剂的氧化性大于氧化产物的氧化性;
D.①中X得到电子被还原.
解答 解:①16H++10Z-+2XO4-═2X2++5Z2+8H2O中,Z元素的化合价升高,X元素的化合价降低;
②2A2++B2═2A3++2B-中,A元素的化合价升高,B元素的化合价降低;
③2B-+Z2═B2+2Z-中,B元素的化合价升高,Z元素的化合价降低,则
A.氧化剂的氧化性大于氧化产物的氧化性,则氧化性XO4->Z2>B2>A3+,可发生反应Z2+2A2+=2A3++2Z-,氧化性Z2>A3+,故A正确;
B.①中Z元素的化合价升高,③中Z元素的化合价降低,分别作还原剂、氧化剂,故B错误;
C.氧化剂的氧化性大于氧化产物的氧化性,则氧化性XO4->Z2>B2>A3+,故C正确;
D.①中X得到电子被还原,则X2+是XO4-的还原产物,故D正确;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、基本概念为解答的关键,侧重分析与应用能力的考查,注意氧化性的比较方法,题目难度不大.

练习册系列答案
相关题目
1.已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的是( )
| A. | X的能量一定高于M,Y的能量一定高于N | |
| B. | 因该反应为放热反应,故不必加热就可以发生 | |
| C. | X和Y的总能量一定高于M和N的总能量 | |
| D. | 破坏反应物中的化学键所吸收的能量大于形成生成物中的化学键所放出的能量 |
18.下列有关化学用语使用正确的是( )
| A. | 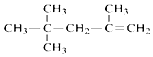 的名称为:2,4,4-三甲基-1-戊烯 的名称为:2,4,4-三甲基-1-戊烯 | |
| B. | 乙酸、葡萄糖、淀粉的最简式均为CH2O | |
| C. | 醛基的电子式: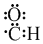 | |
| D. | 乙醇分子比例模型: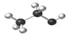 |
5.已知常温下,几种氢氧化物开始沉淀和完全沉淀的pH如表所示:
某矿渣所含各物质的质量分数如表所示:
已知常温下,几种氢氧化物开始沉淀和完全沉淀的pH如表所示:
某课题组拟以上述矿渣为原料制备金属镁、铝、铜、铁,其部分工艺流程如图:
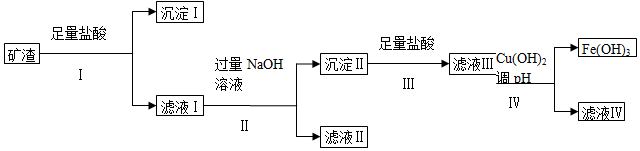
请回答下列问题:
(1)沉淀Ⅰ的主要用途是制光导纤维(列一种即可),步骤Ⅳ中调节pH范围为大于3.7小于4.8.
(2)由滤液Ⅱ经几步反应可得到需要制备的一种金属的氧化物,滤液Ⅱ中需要通入气体的化学式CO2,反应的化学方程式为NaAlO2+CO2+H2O═NaHCO3+Al(OH)3↓,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O.
(3)写出由滤液Ⅰ得到滤液Ⅱ的离子方程式Al3++4OH-═AlO2-+2H2O.
(4)滤液Ⅳ中含有的金属阳离子是Mg2+、Cu2+.
(5)工业上,冶炼铝、铁、铜、镁的方法依次是B(填代号).
A.电解法、热还原法、分解法、分解法 B.电解法、热还原法、热还原法、电解法
C.热还原法、分解法、电解法、电解法 D.热还原法、热还原法、热还原法、电解法
在工业生产中,冶炼这些金属时选择的相应物质的化学式依次是Al2O3、Fe2O3、CuO、MgCl2.
某矿渣所含各物质的质量分数如表所示:
| 成分 | SiO2 | MgO | Fe2O3 | Al2O3 | CuO |
| 质量分数(%) | ? | 4.0 | 32 | 10.2 | 16 |
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |

请回答下列问题:
(1)沉淀Ⅰ的主要用途是制光导纤维(列一种即可),步骤Ⅳ中调节pH范围为大于3.7小于4.8.
(2)由滤液Ⅱ经几步反应可得到需要制备的一种金属的氧化物,滤液Ⅱ中需要通入气体的化学式CO2,反应的化学方程式为NaAlO2+CO2+H2O═NaHCO3+Al(OH)3↓,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O.
(3)写出由滤液Ⅰ得到滤液Ⅱ的离子方程式Al3++4OH-═AlO2-+2H2O.
(4)滤液Ⅳ中含有的金属阳离子是Mg2+、Cu2+.
(5)工业上,冶炼铝、铁、铜、镁的方法依次是B(填代号).
A.电解法、热还原法、分解法、分解法 B.电解法、热还原法、热还原法、电解法
C.热还原法、分解法、电解法、电解法 D.热还原法、热还原法、热还原法、电解法
在工业生产中,冶炼这些金属时选择的相应物质的化学式依次是Al2O3、Fe2O3、CuO、MgCl2.
15.配制0.1mol/L CuSO4溶液1L,正确的操作是( )
| A. | 取25 g CuSO4•5H2O溶于1 L水中 | |
| B. | 取16 g CuSO4•5H2O溶于少量水中,再稀释至1 L | |
| C. | 取16 g无水CuSO4溶于1 L水中 | |
| D. | 取25 g CuSO4•5H2O溶于水配成1 L溶液 |
19.将12g由Mg、Zn、Fe组成的混合物与50mL稀硫酸恰好完全反应,产生的氢气在标准状况下为5.6L,则三种金属的物质量之和为( )
| A. | 0.5mol | B. | 0.25mol | C. | 0.1mol | D. | 0.125mol |
17.某有机物的结构简式为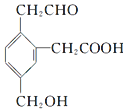 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦缩聚.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦缩聚.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤⑦ | D. | ②③④⑤⑥ |