题目内容
2.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:(1)写出该反应的离子方程式:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O.
(2)下列三种情况下,离子方程式与(1)相同的是A( 填序号).
A.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至过量
(3)若Ba(OH)2溶液中缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度 I 表示)可近似地用如图1中的C (填序号)曲线表示.
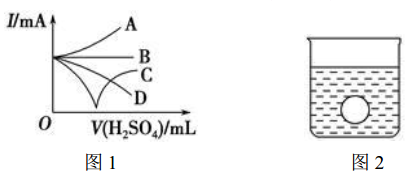
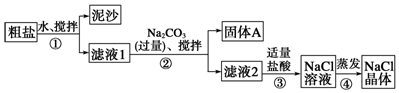
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图2所示.向该烧杯中缓缓注入与 Ba(OH)2溶液等密度的稀硫酸至恰好完全反应.在此实验过程中,小球将下降.( 填“上升”、“下降”或“保持不动”)
分析 (1)氢氧化钡与硫酸反应生成硫酸钡沉淀;
(2)A.NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,反应生成硫酸钠、硫酸钡和水;
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,反应生成硫酸钡、氢氧化钠和水;
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,反应生成硫酸钡、氢氧化钠和水;
(3)加入稀硫酸直至过量,恰好反应时导电性为0,过量后离子浓度增大,导电性增强;
(4)向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应,生成硫酸钡和水,溶液的密度小于Ba(OH)2溶液的密度,以此来解答.
解答 解:(1)向Ba(OH)2溶液中逐滴加入稀硫酸,离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故答案为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
(2)A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O,故B错误;
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O,故C错误;
故选:A;
(3)加入稀硫酸直至过量,恰好反应时导电性为0,过量后离子浓度增大,导电性增强,图中只有C符合,
故答案为:C;
(4)向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应,生成硫酸钡和水,溶液的密度小于Ba(OH)2溶液的密度,塑料小球将沉到烧杯底部,
故答案为:下降.
点评 本题考查离子反应方程式的书写,为高考常见的题型,题目难度中等,涉及与量有关的离子反应、导电性等,把握反应的实质即可解答,试题有利于培养学生灵活应用所学知识的能力.

| A. | 冰水混合物是纯净物 | B. | 金属氧化物均为碱性氧化物 | ||
| C. | Fe(OH)3胶体带正电 | D. | 同种元素组成的物质一定是纯净物 |
| A. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe2++Cu | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ | |
| D. | 硝酸银与盐酸反应:AgNO3+Cl-═NO3-+AgCl↓ |
①16H++10Z-+2XO4-═2X2++5Z2+8H2O
②2A2++B2═2A3++2B-
③2B-+Z2═B2+2Z-
根据上述反应,判断下列结论中错误的是( )
| A. | 溶液中可能发生反应Z2+2A2+=2A3++2Z- | |
| B. | Z2在①③反应中作还原剂 | |
| C. | 氧化性强弱顺序为XO4->Z2>B2>A3+ | |
| D. | X2+是XO4-的还原产物 |
| A. | 150mL1mol/L NaCl溶液 | B. | 75mL2mol/L NH4Cl溶液 | ||
| C. | 150mL3mol/L KCl溶液 | D. | 75mL1mol/L CuCl2溶液 |
| A. | 碘的升华 | B. | 金属的焰色反应 | C. | 液溴的气化 | D. | 漂白粉久置失效 |
| A. | 沸点:NH3>H2O>HF | B. | 熔点:金刚石>碳化硅>晶体硅 | ||
| C. | 硬度:白磷>冰>二氧化硅 | D. | 熔点:SiI4<SiBr4<SiCl4 |
| A. | 密度小 | B. | 强度高 | C. | 不易生锈 | D. | 导电性好 |
请回答下列问题:
(1)步骤①和②的操作名称是过滤.
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡产生为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止溶液飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | Ⅰ有气泡放出,澄清石灰水变浑浊 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入Ⅱ稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | Ⅲ猜想Ⅱ不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,Ⅳ滴入BaCl2溶液和稀HNO3溶液 | Ⅴ有白色沉淀且不溶于稀HNO3 | 猜想Ⅲ成立 |