题目内容
已知,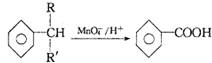 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到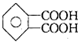 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )
 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )| A、2种 | B、3种 | C、4种 | D、5种 |
考点:常见有机化合物的结构,有机化合物的异构现象
专题:同分异构体的类型及其判定
分析:从题意可知,该苯的同系物的各同分异构体的苯环上有2个位于相邻位置的侧链,根据碳原子数守恒,侧链可以是甲基和丁基,乙基和丙基,结合烷基R中直接与苯环连接的碳原子有C-H键来解答.
解答:
解:由题意可知,该苯的同系物的各同分异构体的苯环上有2个位于相邻位置的侧链,根据碳原子数守恒,侧链可以是甲基和丁基,甲基有1种,丁基有4种,其中1种无氢,则苯的同系物有3种,可以是乙基和丙基,乙基有1种,丙基有2种,则苯的同系物有2种,则该有机物可能的结构有5种,故选D.
点评:本题主要考查结构推断、同分异构体书写,关键根据信息判断含有1个苯环及侧链结构的书写,难度较大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A、常温常压下,22.4 L Cl2与足量的铁粉反应,转移的电子数目为2NA |
| B、常温常压下,4 g CH4含有NA个C-H键 |
| C、常温常压下,92 g的NO2和N2O4混合气体中含有的原子数目为6NA |
| D、分子总数为NA的SO2和CO2混合气体中含有的氧原子数目为2NA |
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).不能判断该分解反应已经达到化学平衡的是( )
| A、密闭容器中二氧化碳的体积分数不变 |
| B、密闭容器中气体的总物质的量不变 |
| C、密闭容器中混合气体的密度不变 |
| D、v(NH3)正=2 v(CO2)逆 |
下列涉及的有机物及有机反应类型正确的是( )
| A、乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
| B、葡萄糖、蛋白质、纤维素都能发生水解反应 |
| C、苯乙烯,氯乙烯,乙二醇均可做加聚反应的单体 |
| D、苯与甲苯都是芳香烃,均可以使酸性高锰酸钾褪色 |
某化合物A的分子式C8H8O2.A分子中只含一个苯环且苯环上只有一个取代基,实验表明A的分子上有“C=O”和“C-O-C”等连接形式.关于A的下列说法中,正确的是( )
| A、符合题中A分子结构特征的有机物只有一种 |
| B、A在一定条件下可与4mol H2发生加成反应 |
| C、A分子一定属于酯类化合物,在一定条件下能发生水解反应 |
| D、与A属于同类化合物的同分异构体只有2种 |
100℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、0.1mol/L的醋酸溶液中C(H+)=1×10-1mol/L |
| B、小苏打溶液中:C(Na+)=C(HCO3-) |
| C、KCl溶液中:C(H+)+C(K+)=C(0H-)+C(Cl-) |
| D、PH=12的KOH溶液中:C(OH-)=1×10-2mol/L |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol由CO2和O2组成的混合物气体中含氧原子数为2NA |
| B、0.012千克石墨晶体中含共用电子对数目为2NA |
| C、标准状况下,NA个SO3分子所占的体积约为22.4L |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极溶解的铜的质量为64g |
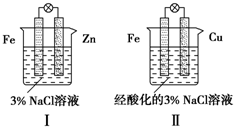 K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )
K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )| A、Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ |
| B、Ⅰ和Ⅱ中正极均被保护 |
| C、Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- |
| D、Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |
能证明Al2O3属离子化合物的是( )
| A、熔融时能导电 |
| B、可作耐火材料 |
| C、受热难分解 |
| D、能溶于NaOH溶液 |