题目内容
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol由CO2和O2组成的混合物气体中含氧原子数为2NA |
| B、0.012千克石墨晶体中含共用电子对数目为2NA |
| C、标准状况下,NA个SO3分子所占的体积约为22.4L |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极溶解的铜的质量为64g |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、由CO2和O2组成的混合物气体中二氧化碳和氧气中氧原子为2个分析;
B、依据石墨结构计算共用电子对数;
C、标准状况三氧化硫不是气体;
D、电解精炼铜时,阳极溶解的是铜、铁、锌、镍等金属,结合电子守恒分析.
B、依据石墨结构计算共用电子对数;
C、标准状况三氧化硫不是气体;
D、电解精炼铜时,阳极溶解的是铜、铁、锌、镍等金属,结合电子守恒分析.
解答:
解:A、每个CO2分子和O2分子都包含2个氧原子,因此1mol由CO2和O2组成的混合物气体中含氧原子数为2NA,故A正确;
B、依据石墨结构计算共用电子对数,0.012千克石墨晶体物质的量为1mol,每六个碳原子形成六个共价键,每个共价键为两个六元环共有,所以1mol石墨中含共用电子对数目为3NA,故B错误;
C、标准状况三氧化硫不是气体,故C错误;
D、电解精炼铜时,阳极首先溶解的是铜、铁、锌、镍等比铜活泼的金属,结合电子守恒分析,电解精炼铜时,若阴极得到电子数为2NA个,则阳极溶解的铜的质量小于64g,故D错误;
故选A.
B、依据石墨结构计算共用电子对数,0.012千克石墨晶体物质的量为1mol,每六个碳原子形成六个共价键,每个共价键为两个六元环共有,所以1mol石墨中含共用电子对数目为3NA,故B错误;
C、标准状况三氧化硫不是气体,故C错误;
D、电解精炼铜时,阳极首先溶解的是铜、铁、锌、镍等比铜活泼的金属,结合电子守恒分析,电解精炼铜时,若阴极得到电子数为2NA个,则阳极溶解的铜的质量小于64g,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是物质结构分析,去摩尔体积条件分析应用,电解精炼原理应用,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质中含有离子键的是( )
| A、Br2 |
| B、CO2 |
| C、NH4Cl |
| D、HNO3 |
若用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、1L1mol/L Na2CO3溶液中含有NA个CO32- |
| B、1mol NH4+有4NA个N-H键 |
| C、标准状况下,46g乙醇的体积为22.4L |
| D、16g O3气体有NA个氧原子 |
已知,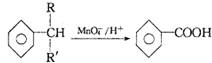 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到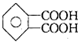 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )
 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )| A、2种 | B、3种 | C、4种 | D、5种 |
在标准状况下,1L氧气约含有n个分子,则阿伏加德罗常数的值可表示为( )
| A、n/22.4 | B、n/32 |
| C、n/16 | D、22.4n |
美国宇航局在2012年再次登陆火星,新火星车体积更大、功能更全,旨在探寻火星土壤中是否存在有机物.已有资料表明:火星表面富含碳酸盐和硫酸盐;火星上的水以冰块和霜冻的形式存在于南北两极.下列叙述不正确的是( )
| A、碳酸盐、硫酸盐都是含氧酸盐 |
| B、空气是混合物,冰水混合物是纯净物 |
| C、硫酸盐一定易溶于水 |
| D、碳酸钠、硫酸钠均属于钠盐 |
NA表示阿伏加德罗常数的值,下列有关说法正确的是( )
| A、标准状况下,22.4 LCH4和CH3CH2OH的混合物所含分子数为NA |
| B、常温常压下,16 g14CH4所含中子数目为8 NA |
| C、0.2 mol的Na2O2和水完全反应转移的电子数为0.2 NA |
| D、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
下列变化过程中.所需克服的作用力均相同的是( )
| A、水气化 氯化钠熔化 |
| B、一冰升华 加热氯化按 |
| C、过氧化氢加入二氧化锰制氧气 碘化氢气体受热分解 |
| D、大理石高温生成二氧化碳.碘晶体升华为碘蒸气 |
下列数量的物质中,含原子数最多的是( )
| A、标准状况下11.2L CO2 |
| B、0.2mol NH3 |
| C、13.5g水 |
| D、6.02×1023个Ar原子 |