题目内容
3.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1molH2O所含有的原子数为NA | |
| B. | 32gO2含有的氧原子数为2NA | |
| C. | 常温常压下,11.2 LCl2 所含的分子数为0.5NA | |
| D. | 1L0.1mol/LNaCl溶液中所含的Na+数为NA |
分析 A.1个水分子含有3个原子;
B.依据n=$\frac{m}{M}$计算解答;
C.常温常压,Vm≠22.4L/mol;
D.依据n=CV计算.
解答 解:A.1molH2O含有3mol原子,所含有的原子数为3NA,故A错误;
B.32gO2含有的氧原子数为$\frac{32g}{32g/mol}$×2×NA=2NA,故B正确;
C.常温常压,Vm≠22.4L/mol,无法计算氯气的物质的量和分子数,故C错误;
D.1L0.1mol/LNaCl溶液中所含的Na+数为1L×0.1mol/L×NA=0.1NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
相关题目
14.下列叙述正确的是( )
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7 | |
| C. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力相当 | |
| D. | 25℃时,将等体积pH=1的盐酸和和水混合,混合后溶液的pH=1.3 |
11.在相同条件下,下列各组物质中,分子数最多的是( )
| A. | 14g N2 | B. | 4g H2 | ||
| C. | 标准状况下11.2L CO2 | D. | 0.5mol O2 |
18.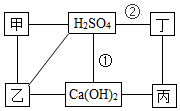 图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种,下列说法正确的是( )
图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种,下列说法正确的是( )
 图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种,下列说法正确的是( )
图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种,下列说法正确的是( )| A. | 甲是Na2CO3 | B. | 乙是Mg | ||
| C. | 反应①②是非氧化还原反应 | D. | 丙与丁发生反应时,丁是还原剂 |
8.雾霾天气中SO2是造成空气污染的主要原因;在硫酸工业生产过程中2SO2(g)+O2(g)?2SO3(g)是关键步骤.该反应的过程在600℃时的平衡常数K=19,有关的能量变化,实验数据如图所示.
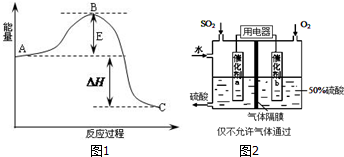
(1)已知1mol SO2(g)氧化为1mol SO3(g)时的△H=-99kJ/mol.则图中△H=198 kJ/mol; E代表的意义是正反应活化能.结合表中的数据解释该反应是放热反应的原因:压强一定时,温度升高,SO2转化率下降,说明升温有利于逆反应进行,所以正反应为放热反应;若600℃时,在一密闭容器中,将二氧化硫和氧气混合,当测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,化学反应速率是v(正)> v(逆)(填“>”、“<”或“=”).
(2)硫酸工厂尾气处理时用NaOH溶液吸收SO2生成NaHSO3.已知在0.1mol/L的NaHSO3溶液中有关微粒浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3).该溶液中c(H+)>c(OH-)(填“>”、“<”或“=”),简述理由(用简单的文字和离子方程式说明):NaHSO3溶液中存在反应:HSO3-?H++SO32-、HSO3-+H2O?OH-+H2SO3,由于c(SO32-)>c(H2SO3),所以电离程度大于水解.
(3)有人设想用电化学原理生产硫酸(装置见图2),写出通入SO2的电极的电极反应式:SO2+2H2O-2e-=SO42-+4H+;为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为16:29.

| 压强/Mpa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)硫酸工厂尾气处理时用NaOH溶液吸收SO2生成NaHSO3.已知在0.1mol/L的NaHSO3溶液中有关微粒浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3).该溶液中c(H+)>c(OH-)(填“>”、“<”或“=”),简述理由(用简单的文字和离子方程式说明):NaHSO3溶液中存在反应:HSO3-?H++SO32-、HSO3-+H2O?OH-+H2SO3,由于c(SO32-)>c(H2SO3),所以电离程度大于水解.
(3)有人设想用电化学原理生产硫酸(装置见图2),写出通入SO2的电极的电极反应式:SO2+2H2O-2e-=SO42-+4H+;为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为16:29.
6.2015年末,在巴黎召开的全球气候变化大会讨论了“全球气温升高过快”的议题.该议题的实质是如何减少排放下列气体中的( )
| A. | H2 | B. | CO2 | C. | N2 | D. | O2 |