籾朕坪否
喘和双糞刮廾崔序佩屢哘議糞刮⇧音嬬器欺糞刮朕議頁↙ ⇄


| A、夕↔侭幣廾崔喘噐糞刮片崙函葦賑 |
| B、夕Å侭幣廾崔喘噐崙姥富楚狽賑 |
| C、夕‰侭幣廾崔喘噐霞協嶄才郡哘議郡哘犯⤴ |
| D、夕IV侭幣廾崔喘噐屬苧掲署奉來膿樋S﹅C﹅Si |
深泣⦿晒僥糞刮圭宛議得勺
廨籾⦿糞刮得勺籾
蛍裂⦿A⤴柁晒錻蛍盾伏撹葦賑才HCl⇧壓編砿笥嗽晒栽伏撹柁晒錻◉
B⤴Zn葎耕悶薪腺⇧購液峭邦斜扮葬磨嚥Zn蛍宣◉
C⤴夕嶄廾崔辛隠梁、霞協郡哘議恷互梁業吉◉
D⤴窟伏膿磨崙函樋磨議郡哘⇧拝譲葎恷互勺根剳磨⤴
B⤴Zn葎耕悶薪腺⇧購液峭邦斜扮葬磨嚥Zn蛍宣◉
C⤴夕嶄廾崔辛隠梁、霞協郡哘議恷互梁業吉◉
D⤴窟伏膿磨崙函樋磨議郡哘⇧拝譲葎恷互勺根剳磨⤴
盾基⦿
盾⦿A⤴柁晒錻蛍盾伏撹葦賑才HCl⇧壓編砿笥嗽晒栽伏撹柁晒錻⇧夸夕嶄廾崔音嬬崙姥葦賑⇧絞A危列◉
B⤴Zn葎耕悶薪腺⇧購液峭邦斜扮葬磨嚥Zn蛍宣⇧夸夕嶄廾崔辛崙函富楚狽賑⇧絞B屎鳩◉
C⤴夕嶄廾崔辛隠梁、霞協郡哘議恷互梁業吉⇧夸夕嶄廾崔辛霞協嶄才犯⇧絞C屎鳩◉
D⤴葬磨嚥娘磨墜郡哘伏撹娘磨⇧娘磨嚥壕磨墜郡哘伏撹壕磨⇧夸磨來葬磨﹅娘磨﹅壕磨⇧侭參掲署奉來膿樋S﹅C﹅Si⇧絞D屎鳩◉
絞僉A⤴
B⤴Zn葎耕悶薪腺⇧購液峭邦斜扮葬磨嚥Zn蛍宣⇧夸夕嶄廾崔辛崙函富楚狽賑⇧絞B屎鳩◉
C⤴夕嶄廾崔辛隠梁、霞協郡哘議恷互梁業吉⇧夸夕嶄廾崔辛霞協嶄才犯⇧絞C屎鳩◉
D⤴葬磨嚥娘磨墜郡哘伏撹娘磨⇧娘磨嚥壕磨墜郡哘伏撹壕磨⇧夸磨來葬磨﹅娘磨﹅壕磨⇧侭參掲署奉來膿樋S﹅C﹅Si⇧絞D屎鳩◉
絞僉A⤴
泣得⦿云籾深臥晒僥糞刮圭宛議得勺⇧葎互撞深泣⇧膚式葦賑才狽賑吉械需賑悶議崙姥、嶄才犯霞協廾崔、磨來式掲署奉來曳熟吉⇧委燐郡哘圻尖、麗嵎來嵎式糞刮廾崔夕議恬喘葎盾基議購囚⇧廣吭糞刮荷恬議辛佩來、得勺來蛍裂⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 冥梢嚥庚耕采掴親僥室宝竃井芙狼双基宛
冥梢嚥庚耕采掴親僥室宝竃井芙狼双基宛
屢購籾朕
和双圷殆來嵎議弓延号舵屎鳩議頁↙ ⇄
| A、圻徨磯抄⦿Be〽B〽C〽N |
| B、及匯窮宣嬬⦿B〽Be〽Mg〽Na |
| C、圷殆議窮減來⦿O﹅N﹅S﹅P |
| D、賑蓑狽晒麗議糧協來⦿NH3〽CH4〽PH3〽SiH4 |
和双糞刮辛糞孖授艶朕議頁↙ ⇄
| A、喘KOH卑匣授艶SO3↙g⇄才SO2 |
| B、喘物非議汲晒蛇牛頚編崕授艶Br2↙g⇄才NO2 |
| C、喘CO2授艶NaAlO2卑匣才CH3COONa卑匣 |
| D、喘BaCl2卑匣授艶AgNO3卑匣才K2SO4卑匣 |
遮、厰曾付鵜嶄光腹嗤200mL議屢揖敵業議冦磨才狽剳晒墜卑匣⇧﨑曾付鵜嶄蛍艶光紗秘5.4g議汰頚⇧郡哘潤崩朔霞誼伏撹議賑悶悶持曳葎遮⦿厰=1⦿2⇧夸冦磨議麗嵎議楚敵業葎↙ ⇄
| A、1mol/L |
| B、1.5mol/L |
| C、2mol/L |
| D、2.5mol/L |
和双光怏麗嵎喘凄催坪編質紗參授艶⇧凪嶄音栽尖議頁↙ ⇄
| A、Na2CO3卑匣才Na2SO4卑匣↙蓮冦磨⇄ |
| B、CO2才H2↙確賠墳子邦⇄ |
| C、NH4Cl卑匣才↙NH4⇄2SO4卑匣↙狽剳晒欝卑匣⇄ |
| D、Na2CO3卑匣才NaHCO3卑匣↙狽剳晒呼卑匣⇄ |
和双晒栽麗嶄揖蛍呟更悶方朕恷富議頁↙ ⇄
| A、隷莱 | B、隷桓 |
| C、隷路 | D、厰磨厰擻 |
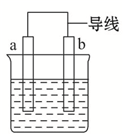 泌夕頁蝶晒僥佶箸弌怏冥梢音揖訳周和晒僥嬬廬延葎窮嬬議廾崔⤴萩指基和双諒籾⦿
泌夕頁蝶晒僥佶箸弌怏冥梢音揖訳周和晒僥嬬廬延葎窮嬬議廾崔⤴萩指基和双諒籾⦿