题目内容
10.已知异丙苯的结构简式如图,下列说法错误的是( )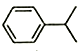
| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯能使酸性高锰酸钾溶液褪色 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯的和苯为同系物 |
分析 A.由有机物结构简式确定元素种类;
B.与苯环相连接的碳原子连接H,可被氧化;
C.含有饱和烃基,具有甲烷的结构特点;
D.异丙苯和苯的结构相似,分子组成上相差3个CH2原子团,互为同系物.
解答 解:A.由有机物结构简式可知有机物的分子式为C9H12,故A正确;
B.与苯环相连接的碳原子连接H,可被氧化,能使酸性高锰酸钾褪色,故B正确;
C.苯环为平面结构,但侧链中存在四面体结构,故C错误;
D.异丙苯和苯的结构相似,分子组成上相差3个CH2原子团,互为同系物,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,注意四面体碳最多3原子共平面,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
5.表是元素周期表的一部分,根据所给的10种元素,完成以下各小题.
(1)镁的原子结构示意图为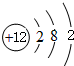 .
.
(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al(OH)3中,属于两性氢氧化物的是Al(OH)3,它常用作治疗胃酸(含盐酸)过多的药物,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(4)碳元素形成的一种氧化物的化学式是CO或CO2,该物质中C元素与O元素的质量比为3:4(或3:8).(相对原子质量:C-12 O-16)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
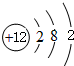 .
.(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al(OH)3中,属于两性氢氧化物的是Al(OH)3,它常用作治疗胃酸(含盐酸)过多的药物,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(4)碳元素形成的一种氧化物的化学式是CO或CO2,该物质中C元素与O元素的质量比为3:4(或3:8).(相对原子质量:C-12 O-16)
15.工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如图:

已知:Cu2O+2H+═Cu+Cu2++H2O
(1)固体混合物A中的成分是SiO2、Cu.
(2)反应Ⅰ完成后,铁元素的存在形式为Fe2+(填离子符号)请写出生成该离子的离子方程式2Fe3++Cu=Cu2++2Fe2+.
(3)x、y对应的数值范围分别是3.2≤pH<4.0、5.2≤pH<5.4.
(4)电解法获取Cu时,阴极反应式为Cu2++2e-=Cu,阳极反应式为2Cl--2e-=Cl2↑.
(5)下列关于NaClO调pH的说法正确的是b.
a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+═HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O═HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO.

已知:Cu2O+2H+═Cu+Cu2++H2O
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)反应Ⅰ完成后,铁元素的存在形式为Fe2+(填离子符号)请写出生成该离子的离子方程式2Fe3++Cu=Cu2++2Fe2+.
(3)x、y对应的数值范围分别是3.2≤pH<4.0、5.2≤pH<5.4.
(4)电解法获取Cu时,阴极反应式为Cu2++2e-=Cu,阳极反应式为2Cl--2e-=Cl2↑.
(5)下列关于NaClO调pH的说法正确的是b.
a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+═HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O═HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO.
2.下列物质属于纯净物的是( )
| A. | 氢氧化铁胶体 | B. | 碘酒 | C. | 胆矾(CuSO4•5H2O ) | D. | 生铁 |
20.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
| A. | v(NO)=0.0010mol•L-1•s-1 | B. | v(O2)=0.0010mol•L-1•s-1 | ||
| C. | v(NH3)=0.0100mol•L-1•s-1 | D. | v(H2O)=0.045mol•L-1•s-1 |
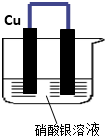 如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.
如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.