题目内容
1.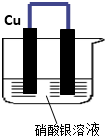 如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.
如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.(1)铁片上的现象是金属逐渐减少,电极反应式Fe-2e-=Fe2+.
(2)铜片上的现象是生成银白的固体,电极反应式2Ag++2e-=2Ag.
(3)写出该电池总反应的离子方程式Fe+2Ag+=2Ag+Fe2+.
分析 该原电池中,Fe易失电子作负极、Cu作正极,负极上电极反应式为Fe-2e-=Fe2+,正极上电极反应式为2Ag++2e-=2Ag,导致负极上金属逐渐减少,正极生成银白的固体,正负极反应之和即为总反应,由此分析解答.
解答 解:该原电池中,Fe易失电子作负极、Cu作正极,负极上电极反应式为Fe-2e-=Fe2+,正极上电极反应式为2Ag++2e-=2Ag,导致负极上金属逐渐减少,正极生成银白的固体,
(1)铁片金属逐渐减少,电极反应式为Fe-2e-=Fe2+,故答案为:金属逐渐减少;Fe-2e-=Fe2+;
(2)铜片上生成银白的固体,电极反应式为2Ag++2e-=2Ag,故答案为:生成银白的固体;2Ag++2e-=2Ag;
(3)电池总反应的离子方程式为:Fe+2Ag+=2Ag+Fe2+,故答案为:Fe+2Ag+=2Ag+Fe2+.
点评 本题考查了原电池,明确正负极的判断方法及电极上发生的反应是解本题关键,根据电极反应确定发生的现象,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列表示对应化学反应的离子方程式正确的是( )
| A. | 氢氧化钡溶液与硫酸铜溶液反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| B. | 向10mL1mol/LNa2CO3溶液中逐滴加入5mL1mol/L盐酸:2H++CO${\;}_{3}^{2-}$═CO2↑+H2O | |
| C. | 将过量SO2通入冷氨水中:SO2+NH3•H2O═HSO${\;}_{3}^{-}$+NH${\;}_{4}^{+}$ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO${\;}_{3}^{-}$═Ag++NO↑+H2O |
9.下列金属中能溶于稀硫酸,但用它制成的容器适合用来盛装浓硫酸的是( )
| A. | 锌 | B. | 铁 | C. | 铜 | D. | 金 |
16.硅被誉为无机非金属材料的主角,硅单质可用来制作( )
| A. | 陶瓷餐具 | B. | 石英表 | C. | 计算机芯片 | D. | 光导纤维 |
10.已知异丙苯的结构简式如图,下列说法错误的是( )
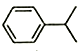

| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯能使酸性高锰酸钾溶液褪色 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯的和苯为同系物 |
11.瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是( )
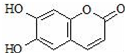

| A. | 与稀H2SO4混合加热不反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol 瑞香素最多能与3mol Br2发生反应 | |
| D. | 1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 2mol |
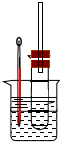 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证

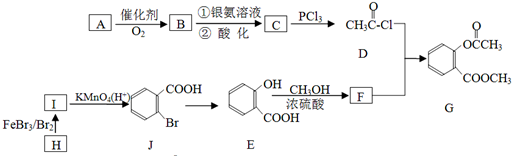
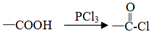
 ;
;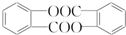 ;
;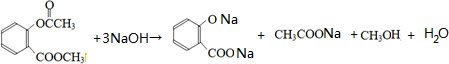 ;
; .
.