题目内容
18.下列物质能导电是①④⑤,属于电解质的是②③④,属于非电解质的是⑥⑦.(填写代号)①Cu ②NaCl晶体 ③CaCO3固体 ④熔融KCl ⑤盐酸溶液 ⑥蔗糖 ⑦CO2.
分析 电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质在水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;非电解质是指:在熔融状态和水溶液中都不能导电的化合物;单质,混合物既不是电解质也不是非电解质;单质和电解质溶液都能导电.
解答 解:①铜是金属单质,能导电;但它既不是电解质也不是非电解质;
②氯化钠由钠离子和氯离子构成,固体没有自由移动的离子,所以不导电;在水溶液中或熔融状态下,能电离出自由移动的钠离子和氢氧根离子导电,是电解质;
③CaCO3是由钙离子和碳酸根离子构成,固体没有自由移动的离子,所以不导电;在水溶液中或熔融状态下,能电离出自由移动的钙离子和碳酸根离子导电,是电解质;
④熔融KCl是由钾离子和氯离子构成,离子能自由移动,故能导电;是电解质;
⑤盐酸溶液中有自由移动的氯离子和氢离子,能导电;但它是氯化氢的水溶液,是混合物,所以,它既不是电解质也不是非电解质;
⑥蔗糖只存在蔗糖分子,没有自由移动的离子,所以不能导电;蔗糖是化合物,在水溶液中和熔融状态下只存在蔗糖分子,没有自由移动的离子,所以不能导电,是非电解质;
⑦CO2由原子构成,无离子,故不能导电;在水溶液中导电和二氧化碳本身无关,在熔融状态下不能导电,故为非电解质.
故答案为:①④⑤;②③④;⑥⑦.
点评 本题重点考查了电解质、非电解质概念的辨析,解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件,单质和电解质溶液都能导电是解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列金属中能溶于稀硫酸,但用它制成的容器适合用来盛装浓硫酸的是( )
| A. | 锌 | B. | 铁 | C. | 铜 | D. | 金 |
10.已知异丙苯的结构简式如图,下列说法错误的是( )
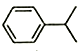

| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯能使酸性高锰酸钾溶液褪色 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯的和苯为同系物 |
8.某溶液中可能含有Na+、Mg2+、Fe2+、H+、OH-、NO3-等几种离子中的若干种,向该溶液中加入氧化铝后,溶液中有X离子生成,下列判断中正确的是( )
| A. | 溶液中可以同时含有Fe2+、NO3- | B. | 溶液中一定有OH-、Na+ | ||
| C. | 溶液中可能含有Na+、H+、Mg2+、NO3- | D. | 若X是AlO2-,则上述离子最多有2种 |
 碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:
碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:

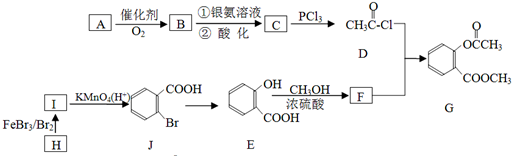
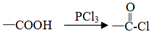
 ;
;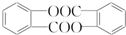 ;
;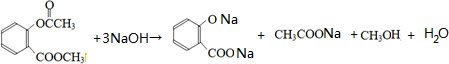 ;
;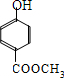 .
.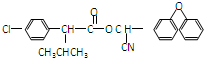 )
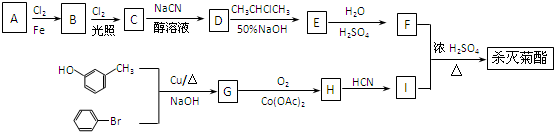
)
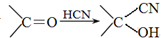
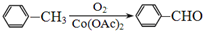
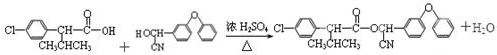 .
.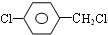 +3NaOH$\stackrel{高温高压}{→}$2NaCl+H2O+
+3NaOH$\stackrel{高温高压}{→}$2NaCl+H2O+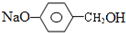
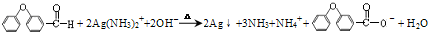
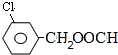 、
、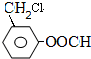 .
.