题目内容
8.过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态.如图1是1mol NO2与1mol CO恰好反应生成CO2和NO过程中的能量变化示意图.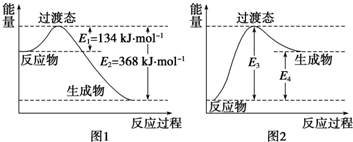
(1)试写出NO2和CO 反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234kJ•mol-1,该反应的活化能是134kJ•mol-1.
(2)图2 是某学生模仿图1 画出的NO(g)+CO2(g)═NO2(g)+CO(g)的能量变化示意图.则图中E3=368kJ•mol-1,E4=234kJ•mol-1.
分析 (1)根据能量变化图,反应热等于正反应的活化能减去逆反应的活化能;
图中E1是活化能,即该反应的活化能为134kJ•mol-1;
(2)E3即为逆反应的活化能,E4是反应物与生成物的能量之差,即为反应热.
解答 解:(1)该反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol,所以热化学方程式为:NO2(g)+CO(g)═NO(g)+CO2(g)
△H=-234kJ•mol-1,图中E1是活化能,即该反应的活化能为134kJ•mol-1;
故答案为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234kJ•mol-1;134;
(2)E3即为逆反应的活化能,即为368KJ/mol,E4是该反应的反应热,即为234KJ/mol,故答案为:368;234.
点评 本题考查了热化学方程式的书写,为高频考点,侧重于学生的分析、计算能力的考查,注意把握图象的意义、正逆反应的反应热数值相等、符号相反,难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
19.将SO2和X气体分别通入BaCl2溶液,未见沉淀生成,若同时通入,有沉淀生成,则X气体可能是( )
| A. | CO2 | B. | SO3 | C. | C12 | D. | HCl |
16.将2.3g金属钠投入到200mL 0.1mol/L氯化铝溶液中,充分反应后,溶液中大量存在的离子有( )
| A. | Na+、Cl-、OH- | B. | Na+、Cl-、OH-、AlO2- | ||
| C. | Na+、Cl-、Al3+ | D. | Na+、Cl-、AlO2-、Al3+ |
3.碰撞理论是一种较直观的反应速率理论,下列有关碰撞理论叙述不正确的是( )
| A. | 反应物分子必须碰撞才有可能发生反应 | |
| B. | 反应速率大小与单位时间内反应物分子间的碰撞次数成正比 | |
| C. | 有效碰撞是活化分子在一定方向上的碰撞 | |
| D. | 活化分子的平均能量称为活化能 |
20.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素叙述正确的是( )
| A. | 气态氢化物的稳定性:D>C | B. | 原子半径:B>A>C>D | ||
| C. | 单质的还原性:B>A | D. | 原子序数:b>a>c>d |
17.下列烷烃:①异丁烷 ②丙烷 ③正戊烷 ④正丁烷 ⑤甲烷中,沸点由低到高的顺序正确的是( )
| A. | ①②③④⑤ | B. | ⑤③④①② | C. | ③④⑤②① | D. | ⑤②①④③ |
 .
.