题目内容
13.(1)写出氯原子的原子结构示意图 .
.(2)氯元素的非金属性强(填“强”或“弱”)于硫元素的非金属性.
(3)写出氯元素、硫元素最高价氧化物对应水合物的化学式并比较酸性强弱HClO4>H2SO4.
分析 (1)依据原子结构示意图的书写要求书写,氯原子是17号元素分为三个电子层,一层2个电子,二层8个电子.三层7个电子,图中小圈表示氯的原子核,圈内数字表示 质子数,弧线表示电子层,弧线上面的数字表示该层的电子数;
(2)氯元素与硫元素在同一周期,结合同周期非金属性的递变规律解答该题;
(3)Cl的最高价为+7价、S的最高价为+6价,非金属性Cl>S,非金属性越强,最高价氧化物对应的水化物酸性越强,以此解答该题.
解答 解:(1)氯原子是17号元素,核外电子分为三个电子层,一层2个电子,二层8个电子.三层7个电子,原子结构示意图为 ,
,
故答案为: ;
;
(2)氯元素和硫元素在同一周期,原子序数Cl>S,因同周期元素从左到右元素的非金属性逐渐增强,则非金属性氯元素强于硫元素,
故答案为:强;
(3)氯元素和硫元素在同一周期,原子序数Cl>S,所以非金属性氯元素强于硫元素,氯元素最高价氧化物对应的水化物为HClO4,硫元素的最高价氧化物对应的水化物为H2SO4,由于非金属性Cl>S,所以其最高价氧化对应的水化物酸性大小为:HClO4>H2SO4 ,
故答案为:HClO4>H2SO4.
点评 本题考查元素周期律的应用等知识,为高频考点,注意掌握原子结构与元素周期律的关系,题目有利于培养学生良好的科学素养,难度不大.

练习册系列答案
相关题目
3.在2000K时,反应CO(g)+$\frac{1}{2}$O2(g)?CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)?2CO(g)+O2(g)的平衡常数为( )
| A. | $\frac{1}{K}$ | B. | K2 | C. | ($\frac{1}{K}$)2 | D. | $(K)^{-\frac{1}{2}}$ |
4.如表实验结论正确的是( )
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条放入氧气瓶中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色固体变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
2.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2$?_{放电}^{充电}$ Cd+2NiO(OH)+2H2O 下列说法正确的是( )
| A. | 该电池放电时负极材料是Cd | B. | 该电池放电时是化学能转化为电能 | ||
| C. | 该电池充电时会消耗NiO(OH) | D. | 该电池充电时Cd(OH)2 会失去电子 |
3.下列各组材料中,不能组成原电池的是( )
| A | B | C | D | |
| 两极材料 | Zn片、石墨 | Cu片、Fe片 | Fe片、石墨 | Fe片、Cu片 |
| 插入溶液 | 稀硫酸 | 浓 HNO3 | FeCl3溶液 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |

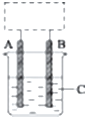 某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4═H2↑+CuSO4(未注明反应条件),试回答:
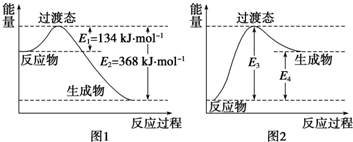
某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4═H2↑+CuSO4(未注明反应条件),试回答: 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.