题目内容
19.(1)下列各实验装置①-⑥,能使我们较长时间观察到白色的氢氧化亚铁沉淀的合理的装置是②③⑤.
(2)把20mL0.05mol•L-1的KMnO4酸性溶液加入到FeSO4溶液中,使紫色全部褪去,则在反应前需要向该KMnO4中加入1mol•L-1的H2SO4不少于4mL.
分析 (1)较长时间观察到白色的氢氧化亚铁沉淀,应防止氢氧化亚铁被氧化,隔绝空气或利用惰性气体保护;
(2)使紫色全部褪去,发生10FeSO4+2KMnO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,以此计算.
解答 解:(1)较长时间观察到白色的氢氧化亚铁沉淀,应防止氢氧化亚铁被氧化,隔绝空气或利用惰性气体保护,由图可知,①中溴可氧化亚铁离子,④中不能隔绝空气,⑥中空气可通过导管进入锥形瓶,只有②③⑤符合,故答案为:②③⑤;
(2)n(KMnO4)=0.02L×0.05mol/L=0.001mol,使紫色全部褪去,由10FeSO4+2KMnO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O可知,消耗硫酸为0.001mol×$\frac{8}{2}$=0.0004mol,其体积为$\frac{0.004mol}{1mol/L}$=0.0004L=4mL,故答案为:4.
点评 本题考查制备实验评价及氧化还原反应的计算,为高频考点,把握氢氧化亚铁的制备反应原理、发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,设计了如图所示的实验装置(其中的夹持仪器没有画出).
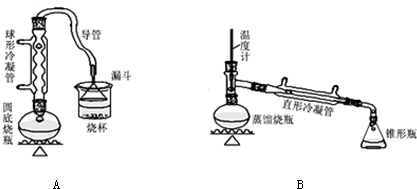
请回答下列问题:
(1)A装置中,在烧杯里的液面倒扣一个漏斗,其目的是既可以吸收充分,又可以防止倒吸.
(2)制备操作中,加入的浓硫酸事先必须进行稀释,其目的是ab.(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.水是反应的催化剂
(3)有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH2CH2CH3”,来确定副产物中是否存在丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3).请评价该同学设计的鉴定方案是否合理?为什么?答:不合理,产物1-溴丁烷也含有-CH2CH2CH2CH3.
(4)为了进一步提纯1-溴丁烷,该小组同学查得相关有机物的有关数据如下表:
则用B装置完成此提纯实验时,实验中要迅速升高温度至101.6℃收集所得馏分.

请回答下列问题:
(1)A装置中,在烧杯里的液面倒扣一个漏斗,其目的是既可以吸收充分,又可以防止倒吸.
(2)制备操作中,加入的浓硫酸事先必须进行稀释,其目的是ab.(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.水是反应的催化剂
(3)有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH2CH2CH3”,来确定副产物中是否存在丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3).请评价该同学设计的鉴定方案是否合理?为什么?答:不合理,产物1-溴丁烷也含有-CH2CH2CH2CH3.
(4)为了进一步提纯1-溴丁烷,该小组同学查得相关有机物的有关数据如下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
10.下列应用或事实与胶体的性质没有关系的是( )
| A. | 用明矾净化饮用水 | |
| B. | 放电影时,放映室射到银幕上的光柱 | |
| C. | 氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 滚滚长江流入大海处,形成长江三角沙洲 |
7. 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )
某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )
 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )
某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )| A. | 烧杯中H2O2溶液作用是将Fe2+氧化为Fe3+ | |
| B. | a中的氧化铁与盐酸反应生成氯化铁 | |
| C. | b中收集到的气体是氢气 | |
| D. | 烧杯中溶液蒸发结晶得到氯化铁晶体 |
4.一定条件下,下列反应呈平衡状态时的平衡常数:K1:3H2+N2?2NH3;K2:NH3?$\frac{3}{2}$H2+$\frac{1}{2}$N2.则K1与K2的关系为( )
| A. | K22=$\frac{1}{{k}_{1}}$ | B. | K1=K2 | C. | K12=K2 | D. | 无法确定 |
11.原电池的正极一定是( )
| A. | 电子流出的极 | B. | 电子流入的极 | ||
| C. | 发生氧化反应的极 | D. | 电极自身参与反应的极 |
9.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | c(H+)=1×10-1 mol•L-1的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| D. | 0.1mol•L-1CH3COONa溶液:H+、Al3+、Cl-、NO3- |
 .
.