题目内容
4.一定条件下,下列反应呈平衡状态时的平衡常数:K1:3H2+N2?2NH3;K2:NH3?$\frac{3}{2}$H2+$\frac{1}{2}$N2.则K1与K2的关系为( )| A. | K22=$\frac{1}{{k}_{1}}$ | B. | K1=K2 | C. | K12=K2 | D. | 无法确定 |
分析 一定条件下,根据平衡常数的定义可知,K1=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,K2=$\frac{{c}^{\frac{3}{2}}({H}_{2})•{c}^{\frac{1}{2}}({N}_{2})}{c(N{H}_{3})}$,据此判断K1与K2的关系.
解答 解:一定条件下,根据平衡常数的定义可知,K1=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,K2=$\frac{{c}^{\frac{3}{2}}({H}_{2})•{c}^{\frac{1}{2}}({N}_{2})}{c(N{H}_{3})}$,所以$\frac{1}{{K}_{1}}$=K22,故选A.
点评 本题主要考查了平衡常数的公式,难度不大,侧重对基础知识的巩固和应用.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
15.物质的量均为0.4mol的钠、镁、铝,分别与50mL 2.0mol/L盐酸反应,则生成的H2在同温同压下的体积比为( )
| A. | 1:1:1 | B. | 1:2:3 | C. | 4:1:1 | D. | 6:3:2 |
12.由硫酸钠、硫酸、硫酸铝组成的混合溶液的pH=1,并且c(SO${\;}_{4}^{2-}$)=0.8mol•L-1,c=(Na+)=0.3mol•L-1,则c(Al3+)为( )
| A. | 0.4mol•L-1 | B. | 0.43mol•L-1 | C. | 0.8mol•L-1 | D. | 1.2mol•L-1 |
16.下列试剂能够使Fe3+转化为Fe2+的是( )
| A. | KSCN溶液 | B. | 氢氧化钠溶液 | C. | 氯水 | D. | 铜粉 |
13.下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A. | 金属氧化物、氧化铁、FeO | B. | 非金属氧化物、二氧化硫、SO2 | ||
| C. | 含氧酸、硫酸、H2SO3 | D. | 碱、纯碱、Na2CO3 |
 .
.
 (1)实验室可以测得下列热化学反应方程式:
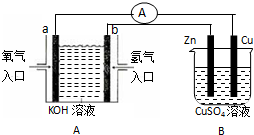
(1)实验室可以测得下列热化学反应方程式: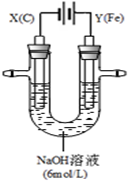 用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.