题目内容
16.NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.己知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,上述反应的氧化剂是NaNO2;若有lmol的氧化剂被还原,则反应中转移电子的数目是6.02×1023.分析 该反应中N元素化合价由+3价变为+2价、部分I元素化合价由-1价变为0价,得电子化合价降低的是氧化剂,失电子化合价升高的反应物是还原剂,结合物质之间的关系式进行计算.
解答 解:该反应中N元素化合价由+3价变为+2价,则NaNO2在反应中得电子化合价降低而作氧化剂,若有lmol的氧化剂被还原,则反应中转移电子的数目是1×(3-2)×6.02×1023=6.02×1023,
故答案为:NaNO2;6.02×1023.
点评 本题考查氧化还原反应,侧重考查基本概念及计算,明确元素化合价变化是解本题关键,难度不大.

练习册系列答案
相关题目
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 400mL 1mol/L稀硝酸与Fe完全反应(还原产物只有NO),转移电子的数目为0.3NA | |
| B. | 含有0.1 mol NH4+的氨水中,含有OH-的数目为0.1 NA | |
| C. | 标准状态下,33.6 L氟化氢中含有1.5 NA个氟化氢分子 | |
| D. | 30 g乙酸和乙酸乙酯的混合物完全燃烧,消耗O2的分子数目为NA |
7.用NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 标准状况下,2.24L水的质量为1.8g | |
| B. | 常温常压下,32gO3含有的原子数为2NA | |
| C. | 11.2L的N2含有的质子数为7NA | |
| D. | 0.1molNa投入到5mL水中转移电子数目为0.2NA |
8.下列仪器名称书写正确的是( )
| A. | 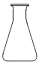 椎形瓶 | B. |  胶头滴管 | C. |  封液漏斗 | D. |  铁夹台 |
5.下列有关金属及其合金的说法不正确的是( )
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 铜的化学性质不活泼,但在潮湿的空气中生锈 | |
| C. | 玻璃钢是复合材料,其中合成树脂做增强体,玻璃纤维做基体 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |