题目内容
12.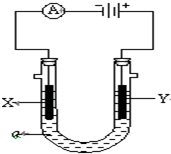 电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为2H++2e-=H2↑.
②Y电极上的电极反应式为2Cl--2e-=Cl2↑,检验该电极反应产物的方法是将湿润的淀粉碘化钾试纸接近出气口,如果试纸变蓝色就说明生成氯气.
③该反应的总反应化学方程式是2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是纯铜,电极反应式是Cu2++2e-=Cu.
②Y电极的材料是粗铜,电极反应式是Cu-2e-=Cu2+.
分析 (1)若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极与电源正极相连为阳极,氯离子放电生成氯气,氯气可以用湿润的淀粉碘化钾试纸检验,X电极上氢离子放电,同时该电极附近生成氢氧根离子;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电,阳极是铜失电子被氧化成铜离子进入溶液中.
解答 解:(1)①若X、Y都是惰性电极,a是饱和NaCl溶液,和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
②若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电生成氯气,电极反应式为2Cl--2e-=Cl2↑,氯气具有氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色,所以氯气可以用湿润的淀粉碘化钾试纸检验,故答案为:2Cl--2e-=Cl2↑;将湿润的淀粉碘化钾试纸接近出气口,如果试纸变蓝色就说明生成氯气;
③X电极上氢离子放电,同时该电极附近生成氢氧根离子,Y电极上氯离子放电生成氯气,所以电池反应式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则与电源负极相连的阴极X是纯铜,阴极是铜离子放电,电极反应式为Cu2++2e-=Cu,与电源正极相连的阳极Y是粗铜,阳极发生反应为:Cu-2e-=Cu2+,
故答案为:纯铜; Cu2++2e-=Cu;粗铜;Cu-2e-=Cu2+.
点评 本题考查原电池原理,为高频考点,侧重于学生的分析能力的考查,本题涉及电极反应式的书写等知识点,注意离子放电顺序及电极反应式的书写,题目难度不大.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 氯气:K+、Na+、AlO2-、CO32- | B. | 二氧化硫:Na+、NH4+、SO32-、Cl- | ||
| C. | 氯化氢:H+、K+、MnO4-、SO42- | D. | 二氧化碳:Mg2+、Al3+、Cl-、NO3- |
| A. | 油脂属于酯类,在酸性或碱性条件下与水发生水解反应,称为皂化反应 | |
| B. | 淀粉、纤维素没有甜味,它们都是天然高分子化合物,在一定条件下水解都能生成葡萄糖 | |
| C. | 鸡蛋清的溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质变性 | |
| D. | 氨基酸分子中都含有-COOH和-NH2二种原子团,能相互反应形成更复杂的多肽化合物 |
| A. | 该反应的还原产物是 I2 | |
| B. | 每生成 1 mol I2,转移的电子为 2 mol | |
| C. | KOH 和 O2 都是还原产物 | |
| D. | 反应中氧化剂与还原剂质量之比为 1:2 |
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2CO3>H2SiO3 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:
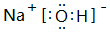 .
.(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)ab.
a.MnO2 b.FeCl3c.Na2SO3d.KMnO4
(5)由①和②两种元素组成的某种物质是天然气的主要成分,该物质4g完全燃烧生成CO2气体和液态水时放出222.5kJ的热量,则该物质燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol
(6)把②和⑥的条状单质用导线相连,放在由①④⑤三种元素组成的化合物的水溶液中,该装置可实现由化学能转化为电能,在该装置中单质⑥做负极,该电极反应式为Al-3e-+4 OH-=AlO2-+2H2O.
 .
.