题目内容
1.臭氧可使湿润的淀粉碘化钾试纸变蓝,化学方程式为:KI+O3+H2O→KOH+I2+O2(未配平),下列叙述正确的是( )| A. | 该反应的还原产物是 I2 | |
| B. | 每生成 1 mol I2,转移的电子为 2 mol | |
| C. | KOH 和 O2 都是还原产物 | |
| D. | 反应中氧化剂与还原剂质量之比为 1:2 |
分析 该反应中碘元素化合价由-1价变为0价,氧元素的化合价由0价变为-2价,根据物质间的关系分析解答,注意臭氧和氧气中化合价相同.
解答 解:A.I元素的化合价升高,在反应中被氧化,则该反应的氧化产物是I2,故A错误;
B.I元素的化合价由-1价升高为0,则每生成1 mol I2,转移的电子为2 mol,故B正确;
C.氧气和臭氧的化合价都是0,所以O2 不是还原产物,故C错误;
D.该反应中KI为还原剂,O3为氧化剂且1 mol O3反应时只有1 mol O原子被还原,则氧化剂与还原剂的物质的量之比为1:2,质量之比为48:2×(127+39)=12:83,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
11.如表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
下列说法正确的是( )
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A. | 甲的金属性比乙强 | B. | 乙的化合价为+1价 | ||
| C. | 丙一定为非金属元素 | D. | 丁一定是金属元素 |
9.下列关于有机物的说法正确的是( )
| A. | “西气东输”中的“气”主要成分是甲烷 | |
| B. | 乙烯的结构简式为CH2CH2 | |
| C. | 分子式为C6H6的物质一定是苯 | |
| D. | 乙烯使溴水褪色说明乙烯与溴发生了取代反应 |
6.X、Y、Z、W为四种短周期主族元素,且原子序数依次增大,其中X、Z同族,Y是短周期主族元素中原子半径最大的,X是农作物生长的三种必须营养元素之一,W的单质以前常用于自来水消毒.下列说法正确的是( )
| A. | Z的最高价氧化物的水化物能形成多种含Y元素的盐 | |
| B. | W的氧化物对应水化物的酸性一定强于Z | |
| C. | Y的单质应该保存在水中 | |
| D. | X的氢化物沸点比Z的氢化物沸点低 |
13.通常人体胃液的pH大约是0.9-1.5.胃液的酸碱性为( )
| A. | 碱性 | B. | 酸性 | C. | 无法判定 | D. | 中性 |
10.金属钠着火时,可采用的灭火物质是( )
| A. | CO2 | B. | 水 | ||
| C. | 干沙 | D. | 干粉(含NaHCO3)灭火剂 |
11.如图为元素周期表中短周期元素的一部分,下列关于Y、Z、M的说法正确的是( )
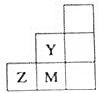

| A. | 非金属性:Y>Z>M | |
| B. | 离子半径:M->Z2->Y- | |
| C. | Z元素存在同素异形现象 | |
| D. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
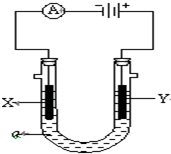 电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: