题目内容
14.已知偏铝酸钡可溶于水,向MgCl2和Al(NO3)3的混合溶液中,逐滴加入Ba(OH)2溶液,其中横坐标表示所加入Ba(OH)2溶液的体积,纵坐标表示反应生成沉淀的质量.则下列图形中,能正确表示上述反应过程的是( )| A. |  | B. |  | C. |  | D. |  |
分析 向MgCl2和Al(NO3)3的混合溶液中,逐滴加入Ba(OH)2溶液,发生反应Mg2++2OH-=Mg(OH)2↓,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,据此分析沉淀随逐滴加入Ba(OH)2溶液的变化分析判断.
解答 解:向MgCl2和Al(NO3)3的混合溶液中,逐滴加入Ba(OH)2溶液,发生反应:Mg2++2OH-=Mg(OH)2↓,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,生成的氢氧化镁沉淀不溶于氢氧化钡溶液,生成的氢氧化铝沉淀是两性氢氧化物,能溶于氢氧化钡溶液,所以沉淀变化为先增大到最大,再减少,最后不变,分析变化可知图象D符合,
故选D.
点评 本题考查了镁铝化合物性质、沉淀生成的变化过程分析判断,主要是氢氧化铝是两性氢氧化物溶于酸碱溶液,题目难度中等.

练习册系列答案
相关题目
15.0.64g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到224mL气体(标况下).将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是( )
| A. | 504mL | B. | 112mL | C. | 336mL | D. | 224mL |
16.常温下,将pH值等于3的酸溶液和pH值等于11的Ba(OH)2溶液等体积混和,所得溶液的pH值( )
| A. | ≥7 | B. | ≤7 | C. | 一定等于7 | D. | 可能大于7 |
2. 石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
 石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )| A. | 3:2 | B. | 2:1 | C. | 1:3 | D. | 2:3 |
19.下列各组物质互为同系物的是( )
| A. | 16O和18O | B. | 正丁烷和异丁烷 | C. | 金刚石和石墨 | D. | CH4和CH3CH3 |
6.Ⅰ.某小组同学对一未知溶液进行了多次检测,其中三次检测结果如下表所示.
(1)三次检测结果中第三次检测结果肯定不正确.
Ⅱ.为了逐一除去溶液中SO42-和Mg2+并且最后所得溶液中不引入新的离子,该组同学选择适当试剂进行实验.可供选择的试剂有:稀HNO3、稀HCl、Ba(OH)2、Ba(NO3)2、NaOH、Na2CO3.相应的实验过程可用下图表示:
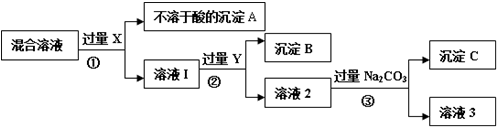
(2)写出实验流程中试剂X的化学式Ba(NO3)2.
(3)上述实验流程中加入过量Na2CO3的目的是使溶液中的Ba2+完全沉淀.
(4)按此实验方案得到的溶液3中肯定引入其他新的阴离子,可以向溶液3中加入适量的稀HNO3除去,写出其中一个反应的化学方程式2HNO3+Na2CO3═2NaNO3+H2O+CO2↑(或HNO3+NaOH=NaNO3+H2O).
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | MgSO4、NaNO3、KNO3、 |
| 第二次 | Mg (NO3)2、KNO3、Na2SO4 |
| 第三次 | Mg (NO3)2、Ba(NO3)2、Na2SO4 |
Ⅱ.为了逐一除去溶液中SO42-和Mg2+并且最后所得溶液中不引入新的离子,该组同学选择适当试剂进行实验.可供选择的试剂有:稀HNO3、稀HCl、Ba(OH)2、Ba(NO3)2、NaOH、Na2CO3.相应的实验过程可用下图表示:

(2)写出实验流程中试剂X的化学式Ba(NO3)2.
(3)上述实验流程中加入过量Na2CO3的目的是使溶液中的Ba2+完全沉淀.
(4)按此实验方案得到的溶液3中肯定引入其他新的阴离子,可以向溶液3中加入适量的稀HNO3除去,写出其中一个反应的化学方程式2HNO3+Na2CO3═2NaNO3+H2O+CO2↑(或HNO3+NaOH=NaNO3+H2O).
 (1)写出Fe2+的最高能层的电子排布式:3s23p63d6.将Fe2O3、KNO3、KOH混合加热共融可制取绿色净水剂K2FeO4,其中KNO3被还原为KNO2,写出该反应的化学方程式Fe2O3+3KNO3+4KOH$\frac{\underline{\;高温\;}}{\;}$2K2FeO4+3KNO2+2H2O.
(1)写出Fe2+的最高能层的电子排布式:3s23p63d6.将Fe2O3、KNO3、KOH混合加热共融可制取绿色净水剂K2FeO4,其中KNO3被还原为KNO2,写出该反应的化学方程式Fe2O3+3KNO3+4KOH$\frac{\underline{\;高温\;}}{\;}$2K2FeO4+3KNO2+2H2O.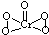 .
.