题目内容
17.原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别为1、5、6、1.a-的电子层结构与氦相同,b和c的次外层电子数与电子层数相同,c2-和d+的电子层结构相同.下列叙述错误的是( )| A. | 元素b、c的离子半径大小为:c<b | |
| B. | a和b、c均能形成电子数为18的分子 | |
| C. | 元素a、b、c各自最高和最低化合价的代数和分别为0、2、4 | |
| D. | d和其他3种元素均能形成离子化合物 |
分析 原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别为1、5、6、1.a-的电子层结构与氦相同,则a为H.b和c的次外层电子数与电子层数相同,二者只能处于第二周期,故b为N,c为O.c2-和d+的电子层结构相同,可推知d为Na.
解答 解:原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别为1、5、6、1.a-的电子层结构与氦相同,则a为H.b和c的次外层电子数与电子层数相同,二者只能处于第二周期,故b为N,c为O.c2-和d+的电子层结构相同,可推知d为Na.
A.N3-、O2-电子层结构相同,核电荷数越大离子半径越小,故离子半径O2-<N3-,故A正确;
B.H和N可以形成N2H4,H与O可以形成H2O2,N2H4、H2O2分子均含有18个电子,故B正确;
C.H元素最高正化合价为+1、最低负化合价为-1,N元素最高正化合价为+5、最低负化合价为-3,二者最高和最低化合价的代数和分别为0、2,氧元素没有最高正化合价+6,故C错误;
D.Na元素与其它元素可以形成KH、Na3N、Na2O,均属于离子化合物,故D正确.
故选:C.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对元素周期律的考查,难度不大,题目涉及金属氢化物是中学知识的盲点.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
7.下列说法正确的是( )
| A. | 硫酸钡不溶于水,所以硫酸钡是非电解质 | |
| B. | 二氧化碳溶于水可以导电,所以,二氧化碳是电解质 | |
| C. | 固态磷酸是电解质,所以磷酸在熔化时或溶于水时都能导电 | |
| D. | 液态氯化氢不能导电,但氯化氢是电解质 |
5.常温下分别将4块形状相同,质量为2.8g的铁块同时投入到下列四种溶液中,铁块首先完全溶解的是( )
| A. | 150 mL 1 mol/L盐酸 | B. | 20 mL 18.4 mol/L硫酸 | ||
| C. | 50 mL 3 mol/L盐酸 | D. | 250 mL 2 mol/L硫酸 |
6.下列物质属于纯净物的是( )
| A. | 酚醛树脂 | B. | 福尔马林 | C. | 葡萄糖 | D. | 纤维素 |
7.化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 | |
| B. | 重金属盐能使蛋白质变性,所以误食重金属盐会中毒 | |
| C. | 在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 | |
| D. | 禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
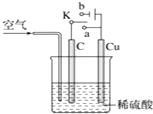 铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题: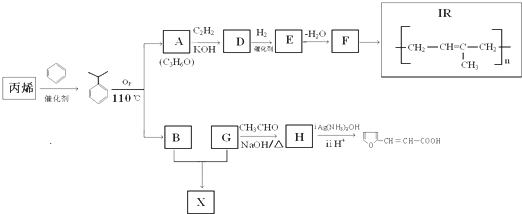
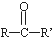 $\stackrel{KOH}{→}$
$\stackrel{KOH}{→}$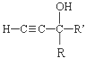
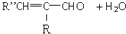 +H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
+H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团) ,反应类型是加成反应.
,反应类型是加成反应. .
. .
. .
.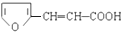 ,符合下列要求的有12种.
,符合下列要求的有12种.