题目内容
1.4℃时,n个水分子的体积为$\frac{18n}{{N}_{A}}$cm3(4℃时,水的密度为1g•cm-3).分析 先根据n=$\frac{N}{{N}_{A}}$计算出n个水分子的物质的量,然后根据m=nM计算出水的质量,最后根据V=$\frac{m}{ρ}$计算出该水的体积.
解答 解:n个水分子的物质的量为:n(H2O)=$\frac{n}{{N}_{A}mo{l}^{-1}}$=$\frac{n}{{N}_{A}}$mol,其质量为:m(H2O)=18g/mol×$\frac{n}{{N}_{A}}$mol=$\frac{18n}{{N}_{A}}$g,
所以该水分子的体积为:V(H2O)=$\frac{m}{ρ}$=$\frac{\frac{18n}{{N}_{A}}g}{1g•c{m}^{-3}}$=$\frac{18n}{{N}_{A}}$cm3,
故答案为:$\frac{18n}{{N}_{A}}$.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列离子方程式书写正确的是( )
| A. | Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | |
| B. | 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| C. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向FeI2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
9.下列反应最终无沉淀产生的是( )
| A. | 过量的CO2通入Na2SiO3溶液中 | |
| B. | 向AlCl3溶液中滴加稀氨水至过量 | |
| C. | 少量的CO2通入BaCl2溶液中 | |
| D. | 向FeCl3溶液中滴加NaOH溶液至过量 |
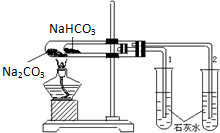 实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答:
实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答: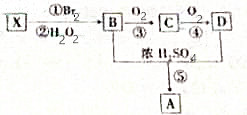 X是一种常见气态烃,它可由乙醇与浓硫酸加热到170℃制得.现以X为主要原料合成一种具有果香味的环状物质A,其合成路线如图所示.其中③、④的催化剂等条件不同;又已知RBr在碱性条件下水解生成ROH.
X是一种常见气态烃,它可由乙醇与浓硫酸加热到170℃制得.现以X为主要原料合成一种具有果香味的环状物质A,其合成路线如图所示.其中③、④的催化剂等条件不同;又已知RBr在碱性条件下水解生成ROH. +2H2O.
+2H2O.