题目内容
4.(1)某含碳、氢、氧三种元素的未知物A,经燃烧分析知其碳的质量分数为60%,氧的质量分数为26.7%,则其实验式为C3H8O;(2)物质A相对于相同状况下的氢气的密度是30,则A的分子式为C3H8O,可能的结构式有3种;
(3)A的红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收,则A的结构简式可能为(有几种写几种)CH3CH2CH2OH,CH3CHOHCH3;
(4)A的核磁共振氢谱有三个吸收峰,峰面积之比为1:1:6,则A的名称是2-丙醇.
分析 (1)碳的质量分数是60%,氧的质量分数是26.7%,氢元素质量分数是1-60%-26.7%=13.3%,根据质量求物质的量,据此写出实验式;
(2)相对分子质量之比等于密度之比,先求出分子量,再根据实验式可知分子式,最后确定结构式;
(3)根据A中有O-H键、C-H键和C-O键解题;
(4)A的核磁共振氢谱有3个峰,说明分子中有3种H原子,其面积之比为对应的各种H原子个数之比.
解答 解:(1)碳的质量分数是60%,氧的质量分数是26.7%,氢元素质量分数是1-60%-26.7%=13.3%,则该物质中碳、氢、氧原子个数之比=$\frac{60%}{12}$:$\frac{13.3%}{1}$%:$\frac{26.7%}{16}$=5:13.3:1.67=3:8:1,所以其实验式为C3H8O,故答案为:C3H8O;
(2)有机物的蒸汽的密度是相同状况下氢气的30倍,可以确定有机物的相对分子质量是60,根据实验式为C3H8O,可知分子式为C3H8O,可能的结构式有CH3CH2CH2OH,CH3CHOHCH3,CH3CH2OCH3,共有3种,故答案为:3;
(3)A中有O-H键、C-H键和C-O键,可能的结构有CH3CH2CH2OH,CH3CH2OHCH3,故答案为:CH3CH2CH2OH,CH3CHOHCH3;
(4)据题意知:有三种峰,说明氢原子有三种情况,峰面积之比是1:1:6,说明这三种氢的个数之比为1:1:6,结构为CH3CHOHCH3,名称是2-丙醇,故答案为:2-丙醇.
点评 本题考查有机物分子式的确定,题目难度较大,本题易错点为根据谱图写出符合条件的结构简式.

练习册系列答案
相关题目
15.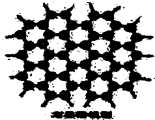 石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
 石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )| A. | 1:3 | B. | 2:3 | C. | 2:1 | D. | 3:2 |
12.区别CH3CH2CH2OH与 的方法是( )
的方法是( )
 的方法是( )
的方法是( )| A. | 加入金属钠 | |
| B. | 加银氨溶液 | |
| C. | 在铜存在下和氧气反应 | |
| D. | 在铜存在下和氧气反应后的产物中加入银氨溶液共热 |
19.如图所示,在较高温度时,钾、氧两元素形成的一种晶体结构与NaCl晶体结构相似,则该化合物的化学式为( )
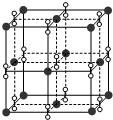

| A. | KO2 | B. | K2O2 | C. | K2O3 | D. | K2O |
9.一定量的乙醇在氧气不足情况下燃烧,得到CO、CO2和H2O的总质量为27.6g,其中水的质量为10.8g,则CO的质量为( )
| A. | 1.4g | B. | 2.2g | C. | 2.8g | D. | 4.4g |
16.下列物质的电子式书写正确的是( )
| A. | 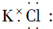 | B. |  | ||
| C. | 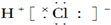 | D. | 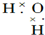 |
