题目内容
16.下列化学用语描述错误的是( )| A. | H2O的电子式? | B. | Cl-的结构示意图 | ||
| C. | NH4Cl为离子化合物 | D. | 质量数为37的氯原子3717Cl |
分析 A、水为共价化合物;
B、氯离子是氯原子得一个电子形成的;
C、所有的铵盐均为离子化合物;
D、在表示原子时,要讲质量数标在元素符号的左上角,质子数标在左下角.
解答 解:A、水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为 ,故A错误;
,故A错误;
B、氯离子是氯原子得一个电子形成的,故核外有18个电子,核内有17个质子,故结构示意图为 ,故B正确;
,故B正确;
C、所有的铵盐均为离子化合物,故氯化铵为离子化合物,由铵根离子和氯离子构成,故C正确;
D、在表示原子时,要讲质量数标在元素符号的左上角,质子数标在左下角,故质量数为37的氯原子为3717Cl,故D正确.
故选A.
点评 本题考查了常用化学用语,熟悉电子式、结构示意图的书写方法,明确水分子含有化学键类型、铵盐的结构特点是解题关键,题目难度不大.

练习册系列答案
相关题目
6.下列变化过程中属于还原反应的是( )
| A. | S2-→HS- | B. | HCO3-→CO2 | C. | 2Cl-→Cl2 | D. | KClO3→KCl |
4.设nA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 1 mol甲苯含有6nA个C-H键 | |
| B. | 18 g H2O含有10nA个质子 | |
| C. | 标准状况下,2.24 L CCl4中含有的C-Cl键数为0.4NA | |
| D. | 常温下,56 g铁片投入足量浓H2SO4中生成nA个SO2分子 |
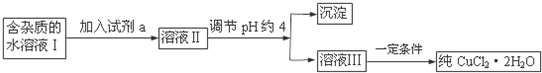
1.现有含FeCl2杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:
25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
请回答下列问题:
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2C.Cu(OH)2D.NaOH
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).理由:加热促进铜离子水解,生成的HCl易挥发,则不能直接蒸发结晶得到CuCl2•2H2O.

25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 4.7 |
| 完成沉淀pH | 3.2 | 9.7 | 6.7 |
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2C.Cu(OH)2D.NaOH
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).理由:加热促进铜离子水解,生成的HCl易挥发,则不能直接蒸发结晶得到CuCl2•2H2O.
8.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 苏打和氢氧化铝胶囊,可以作内服药治疗胃酸过多 | |
| C. | Al2O3和MgO的熔点均很高,可用于制作耐高温材料 | |
| D. | NaHCO3可用作发酵粉、泡沫灭火剂材料、治疗胃酸过多的药物 |
5.下列有关苏打的用途的说法错误的是( )
| A. | 造纸 | B. | 除去油污 | C. | 制肥皂 | D. | 治疗胃酸过多 |
10.已知维生素A的结构简式如图,关于它的叙述中正确的是( )


| A. | 维生素A是一种烯烃 | |
| B. | 维生素A的一个分子中有30个氢原子 | |
| C. | 维生素A的一个分子中有三个双键 | |
| D. | 维生素A能使溴水褪色,能被酸性KMnO4氧化 |