题目内容
等物质的量的烃或烃的含氧衍生物A和B完全燃烧时,消耗氧气的量相等,则A和B的分子量相差不可能为 .
A.18n B.44n C.14n D.26n.
A.18n B.44n C.14n D.26n.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据烃的燃烧化学方程式为CxHy+(x+
)O2
xCO2+
H2O,烃完全燃烧耗氧量由(x+
)值决定,(x+
)的值越大,消耗氧气的量就越多;若为烃的含氧衍生物,物质的量相等的烃CxHy和完全可拆成形式为CxHy?(CO2)m?(H2O)n的烃的衍生物分别完全燃烧后,它们消耗的O2的量相同,据此进行解答.
| y |
| 4 |
| 点燃 |
| y |
| 2 |
| y |
| 4 |
| y |
| 4 |
解答:
解:设烃的化学式为CxHy,燃烧的化学方程式为CxHy+(x+
)O2
xCO2+
H2O,等物质的量的烃完全燃烧耗氧量由(x+
)值决定,(x+
)的值越大,消耗氧气的量就越多,若两种烃的(x+
)相等,耗氧量就相同;
物质的量相等的烃CxHy和完全可拆成形式为CxHy?(CO2)m?(H2O)n的烃的衍生物分别完全燃烧后,它们消耗的O2的量相同,
①当A与B互为同分异构体时,分子式相同,消耗氧气的量相等,则A和B的相对分子质量的差值为0;
②A与B的分子组成只相差n个“CH2”时,即A和B的相对分子质量的差值为14n时,消耗氧气的量不等;
③A与B的分子组成只相差n个“H2O”时,即A和B的相对分子质量的差值为18n时,消耗氧气的量相等;
④A与B的分子组成只相差n个“CO2”时,即A和B的相对分子质量的差值为44n时,消耗氧气的量相等;
⑤A的分子式为CxHy?(H2O)n,B的分子式为CxHy?(CO2)n,二者相对分子质量相差44n-18n=26n,二者消耗的氧气的量相等;
根据以上分析可知,A和B的分子量相差可能为18n、26n、26n,不可能为14n,
故答案为:C.
| y |
| 4 |
| 点燃 |
| y |
| 2 |
| y |
| 4 |
| y |
| 4 |
| y |
| 4 |
物质的量相等的烃CxHy和完全可拆成形式为CxHy?(CO2)m?(H2O)n的烃的衍生物分别完全燃烧后,它们消耗的O2的量相同,
①当A与B互为同分异构体时,分子式相同,消耗氧气的量相等,则A和B的相对分子质量的差值为0;
②A与B的分子组成只相差n个“CH2”时,即A和B的相对分子质量的差值为14n时,消耗氧气的量不等;
③A与B的分子组成只相差n个“H2O”时,即A和B的相对分子质量的差值为18n时,消耗氧气的量相等;
④A与B的分子组成只相差n个“CO2”时,即A和B的相对分子质量的差值为44n时,消耗氧气的量相等;
⑤A的分子式为CxHy?(H2O)n,B的分子式为CxHy?(CO2)n,二者相对分子质量相差44n-18n=26n,二者消耗的氧气的量相等;
根据以上分析可知,A和B的分子量相差可能为18n、26n、26n,不可能为14n,
故答案为:C.
点评:本题考查有机物的燃烧耗氧量的计算,题目难度不大,注意燃烧的化学方程式得出等物质的量的烃完全燃烧耗氧量由(x+
)决定.
| y |
| 4 |

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
用惰性电极电解下列物质的水溶液时,在阳极上不生成O2的是( )
| A、NaOH |
| B、H2SO4 |
| C、ZnCl2 |
| D、Na2SO4 |
将10.4g两种金属的混合物投入足量的盐酸中,反应完全后,得到氢气5.6L(标准状况),该混合物的组成可能是( )
| A、钙和镁 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
下列实验过程中,始终无明显现象的是( )
| A、NO2通入FeSO4溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、Cl2通入Na2CO3溶液中 |
| D、向Na2SiO3溶液中通入过量的CO2气体 |
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:①蒸馏 ②过滤 ③静置分液 ④加入足量的金属钠 ⑤通入过量的二氧化碳 ⑥加入足量的NaOH溶液 ⑦加入足量的FeCl3 溶液 ⑧加入乙酸与浓硫酸混合液加热.合理的实验操作步骤及顺序是( )
| A、④①⑤③ | B、⑥①⑤③ |
| C、⑧①⑦② | D、⑧②⑤③ |
常温下,下列各溶液的叙述中正确的是( )
| A、NaHSO3与Na2SO3混合溶液中一定存在如下关系:2c(Na+)=3(c(HSO3-)+c(SO32-)+c(H2SO3)) |
| B、向0.1mol?L-1的醋酸钠溶液中滴加0.1mol?L-1盐酸至中性,所得溶液中:c (Na+)>c (CH3COO-)>c (Cl-)=c (CH3COOH)>c(H+)=c(OH-) |
| C、等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、向1.00 L 0.3mol?L-1NaOH溶液中缓慢通入0.2molCO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
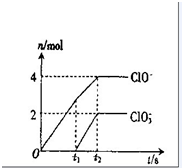 一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中共有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图.生成C1O3-离子的反应为:6Ca(OH)2+6C12═5CaC12+Ca(C1O3)2+6H2O.
一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中共有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图.生成C1O3-离子的反应为:6Ca(OH)2+6C12═5CaC12+Ca(C1O3)2+6H2O.