题目内容
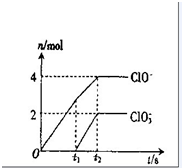 一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中共有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图.生成C1O3-离子的反应为:6Ca(OH)2+6C12═5CaC12+Ca(C1O3)2+6H2O.
一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中共有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图.生成C1O3-离子的反应为:6Ca(OH)2+6C12═5CaC12+Ca(C1O3)2+6H2O.(1)t2时,Ca(C1O)2、Ca(C1O3)2的物质的量之和为
(2)据分析,生成Ca(C1O3)2的反应是由温度升高引起的,通入氯气的速率不同,n(C1O-)和n(C1O3-)的比例也不同. 若在原石灰乳中通入氯气的速率加快,则反应后n(ClO-)/n(ClO3-)
(3)若 n(ClO-)/n(ClO3-)=a,则n(Cl-)=
考点:离子方程式的有关计算
专题:计算题
分析:(1)根据图中数据可以判断次氯酸钙和氯酸钙的物质的量之和,同时能够判断该石灰乳中含有的Ca(OH)2的质量;
(2)根据离子方程式中次氯酸根离子和氢氧化钙物质的量之间的关系式计算.
(3)n(ClO-)/n(ClO3-)=a,根据氯原子守恒可得:an(ClO3-)+n(ClO3-)+n(Cl-)=20,根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),联立方程计算..
(2)根据离子方程式中次氯酸根离子和氢氧化钙物质的量之间的关系式计算.
(3)n(ClO-)/n(ClO3-)=a,根据氯原子守恒可得:an(ClO3-)+n(ClO3-)+n(Cl-)=20,根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),联立方程计算..
解答:
解:(1)氢氧化钙和氯气反应的化学方程式为:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,
6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O,由表中数据可知,次氯酸根离子的物质的量是4mol,说明生成的次氯酸钙的物质的量是2mol,反应的氢氧化钙的物质的量是4mol;氯酸根离子的物质的量是2mol,说明生成的氯酸钙的物质的量是1mol,反应的氢氧化钙的物质的量是6mol,因此t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为3mol;氢氧化钙的物质的量是10mol,质量为:74g/mol×10mol=740g,故答案为:3;740;
(2)若在原石灰乳中通入氯气的速度加快,则反应放热速率加快,温度升高得快,生成氯酸钙的速率加快,导致生成的次氯酸根离子和氯酸根离子的物质的量之比小于2;故答案为:<;
(3)由(2)可知,参加反应的氯气n(Cl2)=n[Ca(OH)2]=10mol,根据氯元素守恒可知,n(ClO-)+n(ClO3-)+n(Cl-)=2n(Cl2)=20mol,若 n(ClO-)/n(ClO3-)=a,则an(ClO3-)+n(ClO3-)=20-n(Cl-),根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),两个方程联立解得:n(Cl-)=
,
故答案为:
.
6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O,由表中数据可知,次氯酸根离子的物质的量是4mol,说明生成的次氯酸钙的物质的量是2mol,反应的氢氧化钙的物质的量是4mol;氯酸根离子的物质的量是2mol,说明生成的氯酸钙的物质的量是1mol,反应的氢氧化钙的物质的量是6mol,因此t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为3mol;氢氧化钙的物质的量是10mol,质量为:74g/mol×10mol=740g,故答案为:3;740;
(2)若在原石灰乳中通入氯气的速度加快,则反应放热速率加快,温度升高得快,生成氯酸钙的速率加快,导致生成的次氯酸根离子和氯酸根离子的物质的量之比小于2;故答案为:<;
(3)由(2)可知,参加反应的氯气n(Cl2)=n[Ca(OH)2]=10mol,根据氯元素守恒可知,n(ClO-)+n(ClO3-)+n(Cl-)=2n(Cl2)=20mol,若 n(ClO-)/n(ClO3-)=a,则an(ClO3-)+n(ClO3-)=20-n(Cl-),根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),两个方程联立解得:n(Cl-)=
| 10(a+5) |
| a+3 |
故答案为:
| 10(a+5) |
| a+3 |
点评:利用图象能够直观地反映物质之间相互作用的过程,因此要学会观察实验数据,善于分析实验数据,有一定的难度.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A、标准状况下,22.4LH2含有的分子数为NA |
| B、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA |
| C、通常状况下,1NA个CO2分子占有的体积为22.4L |
| D、1L0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、金属氧化物 氧化铁 FeO |
| B、非金属氧化物 二氧化氮 NO2 |
| C、酸 硫酸 H2SO3 |
| D、碱 纯碱 Na2CO3 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:

下列说法正确的是( )

下列说法正确的是( )
| A、滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B、样品中Fe元素的质量为2.24 g |
| C、样品中Fe元素的质量为2.49 g |
| D、样品CuO的质量一定为4.0 g |
300℃时,将100mL由H2O、CO2和N2组成的混合气体,通入到盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时,容器内的压强变为原来的四分之三.则原混合气体中N2的体积分数为( )
| A、33.3% | B、25% |
| C、50% | D、75% |
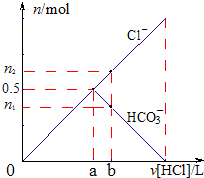 向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2
向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2 大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:
大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如: