题目内容
已知相同条件下碳酸氢根离子的酸性大于氢氧化铝,实验室有A~F六种常见的化合物,它们含有的离子如下:
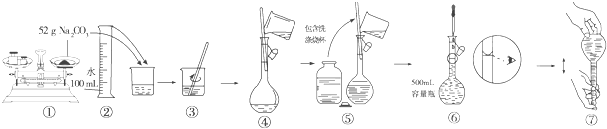
将它们分别配成0.1mol/L的溶液进行如下实验.
①测得溶液A、C、E均呈碱性,且碱性:A>E>C,E的焰色呈浅紫色(透过蓝色钴玻璃观察);
②向B溶液中加稀氨水至过量,先生成沉淀,后沉淀全部溶解;
③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成;
④向D溶液中滴加硝酸钡溶液,无明显现象.
请回答:
(1)C是 (写化学式),该溶液中各离子浓度由大到小的顺序是 ;
(2)写出(3)中的离子反应方程式 ;
(3)写出A与过量的D反应的离子方程式 .
| 阳离子 | K+、Ag+、Na+、Ba2+、Fe2+、Al3+ |
| 阴离子 | Cl-、OH-、AlO2-、NO3-、SO42-、CO32- |
①测得溶液A、C、E均呈碱性,且碱性:A>E>C,E的焰色呈浅紫色(透过蓝色钴玻璃观察);
②向B溶液中加稀氨水至过量,先生成沉淀,后沉淀全部溶解;
③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成;
④向D溶液中滴加硝酸钡溶液,无明显现象.
请回答:
(1)C是
(2)写出(3)中的离子反应方程式
(3)写出A与过量的D反应的离子方程式
考点:无机物的推断,物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:由①溶液A、C、E呈碱性,且碱性为A>E>C可推知A含有OH-、E含有AlO2-、C含有CO32-,E的焰色呈浅紫色,则E为KAlO2;
由②中向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失可推知溶液中含Ag+,则B只能为AgNO3;
由③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成,可知F含Fe2+;
由④向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D溶液中无SO42-,由离子共存知识可推知A、B、C、D、E、F溶液依次为Ba(OH)2、AgNO3、Na2CO3、AlCl3、KAlO2、FeSO4溶液,结合对应物质的性质解答该题.
由②中向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失可推知溶液中含Ag+,则B只能为AgNO3;
由③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成,可知F含Fe2+;
由④向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D溶液中无SO42-,由离子共存知识可推知A、B、C、D、E、F溶液依次为Ba(OH)2、AgNO3、Na2CO3、AlCl3、KAlO2、FeSO4溶液,结合对应物质的性质解答该题.
解答:
解:由①溶液A、C、E呈碱性,且碱性为A>E>C可推知A含有OH-、E含有AlO2-、C含有CO32-,E的焰色呈浅紫色,则E为KAlO2;
由②中向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失可推知溶液中含Ag+,则B只能为AgNO3;
由③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成,可知F含Fe2+;
由④向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D溶液中无SO42-,由离子共存知识可推知A、B、C、D、E、F溶液依次为Ba(OH)2、AgNO3、Na2CO3、AlCl3、KAlO2、FeSO4溶液,
(1)由上述分析可知C为Na2CO3,水解显碱性,且第一步水解远大于第二步水解,则离子浓度大小为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),
故答案为:Na2CO3;c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
(2)亚铁离子与硝酸根离子在酸性条件下发生氧化还原反应,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)A与过量的D反应,碱不足,生成沉淀,其离子方程式为Al3++3OH-═Al(OH)3↓,故答案为:Al3++3OH-═Al(OH)3↓.
由②中向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失可推知溶液中含Ag+,则B只能为AgNO3;
由③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成,可知F含Fe2+;
由④向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D溶液中无SO42-,由离子共存知识可推知A、B、C、D、E、F溶液依次为Ba(OH)2、AgNO3、Na2CO3、AlCl3、KAlO2、FeSO4溶液,
(1)由上述分析可知C为Na2CO3,水解显碱性,且第一步水解远大于第二步水解,则离子浓度大小为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),
故答案为:Na2CO3;c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
(2)亚铁离子与硝酸根离子在酸性条件下发生氧化还原反应,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)A与过量的D反应,碱不足,生成沉淀,其离子方程式为Al3++3OH-═Al(OH)3↓,故答案为:Al3++3OH-═Al(OH)3↓.
点评:本题考查无机物的推断,为高频考点,把握盐类水解、离子之间的反应、氧化还原反应等分析推断物质中的离子为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
化学与环境、生产和生活密切相关.下列说法错误的是( )
| A、化肥的合理使用,缓解了人类粮食危机 |
| B、绿色化学的快速发展,减轻了环境污染 |
| C、新材料的研制和应用,提高了人们的生活品质 |
| D、化石燃料的直接利用,促进了“低碳”经济的发展 |
下列实验设计方案,可行的是( )
| A、检验CO32-,可取少量试剂滴加稀盐酸,若产生无色无味的气体能使澄清石灰水变浑浊,则说明原溶液中一定有CO32- |
| B、检验SO42-,可取少量试剂滴加氯化钡溶液,若产生白色沉淀,则说明原溶液中有SO42- |
| C、用氢氧化钠溶液可除去CO2气体中的HCl气体 |
| D、为除去粗盐中的Ca2+、Mg2+、SO42-可依次加入过量的BaCl2、NaOH、Na2CO3后过滤,再加入适量的稀盐酸 |
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A、合金的熔点一般比组分金属低 |
| B、铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C、铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D、若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
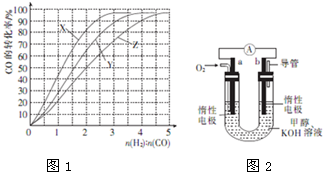
在一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 molCO和1molH2O,在Ⅱ中充入1 molCO2和 1 mol H2,d在Ⅲ中充入2 mol和2 mol H2O.700℃条件下开始反应,达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅱ中反应的平衡常数相同 |
| C、容器Ⅰ中CO的物质的量比容器Ⅱ中的少 |
| D、容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率和小于1 |
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是( )
| A、若反应中转移的电子为nmol,则0.15<n<0.25 |
| B、n(Na+):n(Cl-)可能为7:3 |
| C、与NaOH反应的氯气一定为0.3mol |
| D、n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
下列各组无色溶液中,所含离子能大量共存的是( )
| A、K+ Na+ Cl- NO3- |
| B、Cu2+ H+ HCO3- Cl- |
| C、Na+ Ba2+ Cl- SO42- |
| D、Fe2+ H+ NO3- ClO- |