题目内容
下列实验设计方案,可行的是( )
| A、检验CO32-,可取少量试剂滴加稀盐酸,若产生无色无味的气体能使澄清石灰水变浑浊,则说明原溶液中一定有CO32- |
| B、检验SO42-,可取少量试剂滴加氯化钡溶液,若产生白色沉淀,则说明原溶液中有SO42- |
| C、用氢氧化钠溶液可除去CO2气体中的HCl气体 |
| D、为除去粗盐中的Ca2+、Mg2+、SO42-可依次加入过量的BaCl2、NaOH、Na2CO3后过滤,再加入适量的稀盐酸 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.原溶液中可能含CO32-或HCO3-;
B.沉淀可能为AgCl;
C.氢氧化钠与二氧化碳和氯化氢都反应;
D.除去粗盐中的Ca2+、Mg2+、SO42-,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
B.沉淀可能为AgCl;
C.氢氧化钠与二氧化碳和氯化氢都反应;
D.除去粗盐中的Ca2+、Mg2+、SO42-,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
解答:
解:A.使澄清石灰水变浑浊的无色无味的气体,为二氧化碳,原溶液中可能含CO32-或HCO3-,不能确定未知溶液中一定含有CO32-,故A错误;
B.滴加氯化钡溶液,若产生白色沉淀,溶液中可能含银离子或硫酸根离子,故B错误;
C.氢氧化钠与二氧化碳和氯化氢都反应,不能使用氢氧化钠溶液除去CO2中的HCl气体,故C错误;
D.镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,故D正确.
故选D.
B.滴加氯化钡溶液,若产生白色沉淀,溶液中可能含银离子或硫酸根离子,故B错误;
C.氢氧化钠与二氧化碳和氯化氢都反应,不能使用氢氧化钠溶液除去CO2中的HCl气体,故C错误;
D.镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,故D正确.
故选D.
点评:本题考查物质的检验和物质的分离提纯,为高频考点,把握离子的检验方法、试剂及现象与结论为解答的关键,侧重离子检验的考查,注意检验应排除干扰离子,题目难度不大.

练习册系列答案
相关题目
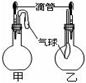 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )| A、甲:铝粉和浓NaOH溶液 乙:饱和NaCl溶液和Cl2 |
| B、甲:双氧水和MnO2 乙:NaOH溶液和CO2 |
| C、甲:浓氨水和碱石灰 乙:浓氨水和SO2 |
| D、甲:水和CO2 乙:水和氯化氢 |
甲、乙、丙、丁四种物质之间存在如图所示转化关系,且甲、乙、丙均含有相同的某种元素.下列推断错误的是( )甲
乙
丙.
| 丁 |
| 丁 |
| 甲 |
| A、若丙为CO2,则甲可以是焦炭 |
| B、若丁为O2,则甲可以是N2 |
| C、若丁为Fe,则甲可以是Cl2 |
| D、若丁为CO2,则甲可以是NaOH溶液 |
利用一种新型陶瓷(能传递H+),实现了氨的电化学合成.该过程N2和H2的转化率远高于现在工业上使用的氨合成法.对于电化学合成氨的有关叙述正确的是( )
| A、N2在阴极上被氧化 | ||||
| B、可选用铁作为阳极材料 | ||||
| C、阳极的电极反应式是N2+6H++6e-═2NH3 | ||||
D、该过程的总反应式是N2+3H2
|
下列有关营养成分与人体健康关系叙述错误的是( )
| A、缺铁会患贫血症 |
| B、为防治佝偻病,过量补钙 |
| C、摄入糖分不足,会患低血糖 |
| D、缺碘人群可多食用海带、虾皮等含碘丰富的食物 |