题目内容
短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和.
(1)元素符号:A为 B为 C为 D为
(2)D在周期表中的位置第 周期 族;它的最高价氧化物对应的水化物的化学式为 .
(3)C与水反应的化学方程式是 ,所得溶液显 (“酸性”或“碱性”).
(1)元素符号:A为
(2)D在周期表中的位置第
(3)C与水反应的化学方程式是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,据此解答.
解答:
解:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,
综上所述:A为碳,B为氧,C为钠,D为硫,
(1)A为C元素、B为O元素、C为Na元素、D为S元素,故答案为:C;O;Na;S;
(2)D为S元素,处于第三周期第ⅥA族,S的最高价氧化物的水化物的化学式是H2SO4,故答案为:三;ⅥA;H2SO4;
(3)钠与水反应生成氢氧化钠与氢气,化学反应方程式为:2Na+2H2O=2NaOH+H2↑,生成的氢氧化钠为碱,显碱性,故答案为:2Na+2H2O=2NaOH+H2↑;碱性.
综上所述:A为碳,B为氧,C为钠,D为硫,
(1)A为C元素、B为O元素、C为Na元素、D为S元素,故答案为:C;O;Na;S;
(2)D为S元素,处于第三周期第ⅥA族,S的最高价氧化物的水化物的化学式是H2SO4,故答案为:三;ⅥA;H2SO4;
(3)钠与水反应生成氢氧化钠与氢气,化学反应方程式为:2Na+2H2O=2NaOH+H2↑,生成的氢氧化钠为碱,显碱性,故答案为:2Na+2H2O=2NaOH+H2↑;碱性.
点评:本题主要考查结构性质位置关系应用,侧重对化学用语的考查,比较基础,注意对基础知识的积累掌握.

练习册系列答案
相关题目
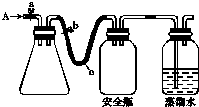 实验室用下列方法测定某水样中O2的含量.
实验室用下列方法测定某水样中O2的含量.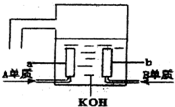
 ).在浓硫酸存在下,A可发生如图所示的反应.
).在浓硫酸存在下,A可发生如图所示的反应.
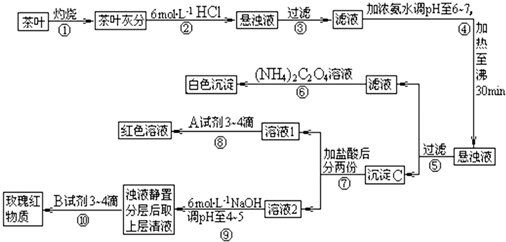
 某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.
某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.