题目内容
19.己烷雌酚的一种合成路线如图: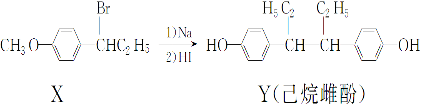
下列叙述正确的是( )
| A. | 在NaOH 水溶液中加热,化合物X 可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与浓溴水发生取代反应 | |
| C. | 用FeCl3溶液不能鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
分析 A.X为卤代烃,在氢氧化钠水溶液中发生水解反应生成醇;
B.Y含有酚羟基,与苯酚性质相似;
C.Y含有酚羟基,可与氯化铁发生显色反应;
D.根据手性碳原子的定义判断.
解答 解:A.X为卤代烃,在氢氧化钠水溶液中发生水解反应生成醇,如发生消去反应,条件为氢氧化钠醇溶液,故A错误;
B.Y含有酚羟基,与苯酚性质相似,可与浓溴水发生取代反应,故B正确;
C.Y含有酚羟基,可与氯化铁发生显色反应,故C错误;
D.连接四个不同的原子或原子团的碳原子为手性碳原子,Y中连接乙基的碳原子为手性碳原子,故D错误.
故选B.
点评 本题为2015年江苏考题第12题改编题,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
9.浓度均为1mol/LNaCl溶液、MgCl2溶液、AlCl3三种溶液中,它们的氯离子的物质的量浓度分别是( )
| A. | 1mol/L 1mol/L 1mol/L | B. | 1mol/L 4mol/L 9mol/L | ||
| C. | 1mol/L 2mol/L 3mol/L | D. | 体积未知,无法确定 |
10. 现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )
现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )
 现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )
现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )| A. | Al、Mg、SiO2、Zn | B. | Al、Fe、Zn、Na | C. | Al、Na、Cu、Fe | D. | Al、Cu、Mg、Si |
7.目前,能较稳定存在的氯的氧化物有Cl2O、ClO2、Cl2O7等.有关数据见表:
请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是Cl2O、ClO2.
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为Cl2O7+H2O=2H++2ClO4-.
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有氧化性.
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法
表示出该反应电子转移的方向和数目.
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是AC(填序号).
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.1molClO2,则转移的电子数为0.1NA.
| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
(1)常温、常压下,三种氧化物中属于气体的是Cl2O、ClO2.
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为Cl2O7+H2O=2H++2ClO4-.
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有氧化性.
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法
表示出该反应电子转移的方向和数目.
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是AC(填序号).
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.1molClO2,则转移的电子数为0.1NA.
4.下列说法正确的是( )
| A. | NaCl晶体中含有Na+、Cl-,所以NaCl晶体能导电 | |
| B. | CO2溶于水能导电,所以CO2是电解质 | |
| C. | BaSO4难溶于水,BaSO4是非电解质 | |
| D. | Cl2的水溶液能够导电,但Cl2既不是电解质也不是非电解质 |
7.海藻中含丰富的、以离子形式存在的碘元素.如图是实验室从海藻里提取碘的流程的一部分下列判断正确的是( )


| A. | 步骤①、③的操作都是过滤 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是精馏 |
8.X(g)+3Y(g)?2Z(g)△H=-a kJ•mol-1,一定条件下,将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol.下列说法正确的是( )
| A. | 10 min内,Y的平均反应速率为0.03 mol•L-1•s-1 | |
| B. | 10 min内,X和Y反应放出的热量为a kJ | |
| C. | 10 min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10 min内,前5minX的平均反应速率与后5minX的平均反应速率相同 |