题目内容
4.下列说法正确的是( )| A. | NaCl晶体中含有Na+、Cl-,所以NaCl晶体能导电 | |
| B. | CO2溶于水能导电,所以CO2是电解质 | |
| C. | BaSO4难溶于水,BaSO4是非电解质 | |
| D. | Cl2的水溶液能够导电,但Cl2既不是电解质也不是非电解质 |
分析 A.氯化钠晶体中不存在自由移动的离子;
B.电解质必须本身能电离产生自由移动离子;
C.硫酸钡熔融状态下能够导电;
D.氯气为单质.
解答 解:A.氯化钠晶体中不存在自由移动的离子,不导电,故A错误;
B.二氧化碳本身不能电离出自由移动的离子,属于非电解质,故B错误;
C.硫酸钡熔融状态下能够导电,是化合物,属于电解质,故C错误;
D.电解质、非电解质必须为化合物,氯气为单质,既不是电解质也不是非电解质,故D正确;
故选:D.
点评 本题考查了电解质的判断,注重了基础知识的考查,题目难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
相关题目
14.原子序数依次增大的前20号元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦原子相同,b和c的次外层均有8个电子,c-和d+的电子层结构相同.下列叙述错误的是( )
| A. | 元素的非金属性强弱:c>b | |
| B. | 元素a和其他3种元素均能形成共价化合物 | |
| C. | 元素d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
15.下列说法不正确的是( )
| A. | 两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 | |
| B. | 常温下,浓度均为0.1mol/L①醋酸、②盐酸、③醋酸钠溶液,水电离程度的顺序为③>①>② | |
| C. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性 | |
| D. | 物质的浓度相同的①氯化铵溶液、②硫酸钠溶液、③碳酸氢钠溶液,pH的顺序为:③>①>② |
12.下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去Fe(OH)3胶体中的FeCl3 | 过滤 | 分散质粒子的大小不同 |
| B | 除去Na2CO3中的NaHCO3 | 加热 | 稳定性不同 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
19.己烷雌酚的一种合成路线如图:
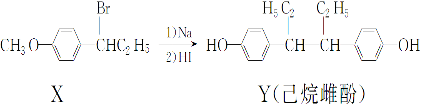
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 在NaOH 水溶液中加热,化合物X 可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与浓溴水发生取代反应 | |
| C. | 用FeCl3溶液不能鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
16.原子序数小于36的四种元素,分别位于不同周期,其中A原子核是一个质子,B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1,下列说法不正确的是( )
| A. | A、B元素形成的一系列化合物中,其中A元素质量分数的最大值为25% | |
| B. | 四种元素中电负性最大的是B | |
| C. | C所形成的气态氢化物,在其同主族元素的气态氢化物中沸点最低 | |
| D. | 四种元素中第一电离能最小的是D |

 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,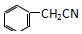 +2H2O+H2SO4$\stackrel{100-130℃}{→}$+NH4HSO4
+2H2O+H2SO4$\stackrel{100-130℃}{→}$+NH4HSO4 ,混合溶剂中乙醇的作用是增大苯乙酸的溶解度,便于充分反应.
,混合溶剂中乙醇的作用是增大苯乙酸的溶解度,便于充分反应.