题目内容
4.用离子方程式解释以下指定反应,书写正确的是( )| A. | 亚硫酸钠溶液显碱性:SO32-+2H2O=H2SO3+2OH- | |
| B. | (NH4)2FeSO4溶液与过量NaOH溶液混合制取氢氧化亚铁:Fe2++2OH-=Fe(OH)2 | |
| C. | NaAlO2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32- | |
| D. | 铁红溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
分析 A.亚硫酸根离子的水解分步进行,水解的离子方程式写出第一步即可;
B.氢氧化钠足量,铵根离子也参与反应;
C.二氧化碳过量,反应生成碳酸氢根离子;
D.二者发生氧化还原反应生成亚铁离子和碘单质.
解答 解:A.亚硫酸钠溶液显碱性,该反应为可逆反应,且水解分步进行,正确的离子方程式为:SO32-+H2O?HSO3-+OH-,故A错误;
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2,铵根离子也参与反应,正确的离子方程式为:2NH4+Fe2++4OH-═Fe(OH)2↓+2NH3•H2O,故B错误;
C.NaAlO2溶液中通入过量CO2,反应生成氢氧化铝和碳酸氢钠,正确的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3+HCO3-,故C错误;
D.铁红溶于HI酸溶液,二者发生氧化还原反应,反应的离子方程式为:Fe2O3+6H++2I-=2Fe2++I2+3H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
15.设NA代表阿伏伽德罗常数(NA)的值,下列说法不正确的是( )
| A. | 1molCa变成Ca2+时失去的电子数为NA | |
| B. | 同温、同压、同体积的CO和NO含有的质子数 | |
| C. | 标准状况下22.4L以任意比例混合的氢气和氧气所含分子总数均为NA | |
| D. | 常温常压下,16g氧气和臭氧(O3)的混合气体中含有NA个氧原子 |
12.NaH与盐酸反应的化学方程式为NaH+HCl=NaCl+H2↑,在该反应中HCl( )
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
19.某化学反应2A?B+D在四种不同条件下进行.B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如表:
根据上述数据,完成下列填空:?
(1)在实验1中,反应在10至20min时间内反应物A的平均速率为0.013.
(2)在实验2中,反应经20min就达到平衡,可推测实验2中还隐含的条件是加入催化剂.??
| 实验 序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min |
| 1 | 820℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 820℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
(1)在实验1中,反应在10至20min时间内反应物A的平均速率为0.013.
(2)在实验2中,反应经20min就达到平衡,可推测实验2中还隐含的条件是加入催化剂.??
9.下列关于元素周期表的说法正确的是( )
| A. | 元素周期表有七个横行,即七个周期 | |
| B. | 元素周期表有十八个竖行,即十八族 | |
| C. | 周期表中有七个主族,十一个副族 | |
| D. | 第ⅠA族又叫卤族 |
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25°C,pH=2的HCl溶液中含有H+的数目为0.01NA | |
| B. | 1mol$NH_4^+$中含有10NA个质子 | |
| C. | 1mol碳烯(:CH2)中含有的电子数8NA | |
| D. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
13.下列碳酸盐中最易分解为氧化物的是( )
| A. | CaCO3 | B. | BaCO3 | C. | MgCO3 | D. | SrCO3 |

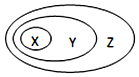 表所列物质或概念间的从属关系符合如图所示关系的是( )
表所列物质或概念间的从属关系符合如图所示关系的是( )