题目内容
4.某元素的一种核素X的质量数为A,含有N个中子,则ag 1HmX分子中所含质子数是6.02×1023×$\frac{a}{A+m}$(A-N+m).分析 X的质量数为A,含N个中子,则质子数为A-N,1HmX分子中质子数为(A-N+m),其摩尔质量为(A+m)g/mol,根据n=$\frac{m}{M}$计算HmX的物质的量,进而得到质子的物质的量,最后带入N=n•NA计算质子数.
解答 解:X的质量数为A,含N个中子,则质子数为A-N,1HmX分子中质子数为(A-N+m),其摩尔质量为(A+m)g/mol,则ag 1HmX的物质的量为$\frac{ag}{(A+m)g/mol}$=$\frac{a}{A+m}$mol,含有质子物质的量为$\frac{a}{A+m}$(A-N+m) mol,所含质子数为$\frac{a}{A+m}$(A-N+m) mol×6.02×1023mol-1=6.02×1023×$\frac{a}{A+m}$(A-N+m)个,
故答案为:6.02×1023×$\frac{a}{A+m}$(A-N+m).
点评 本题考查了物质的量的相关计算,侧重于学生的分析能力和计算能力的考查,注意把握原子构成以及相关物理量的计算公式的运用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列实验操作说法正确的是( )
| 选项 | 实验操作 | 现象与结论(或装置用途) |
| A | 某溶液加入浓NaOH溶液加热,在试管口放一片湿润的红色石蕊试纸 | 试纸变蓝,说明NH3是碱 |
| B | 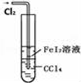 | 可以用于比较Fe3+、I2、Cl2的氧化性强弱 |
| C | 2mL 2% CuSO4中加4~6滴2% NaOH溶液,振荡后加入0.5mL X溶液,加热煮沸 | 未出现砖红色沉淀,说明X不含有醛基 |
| D | 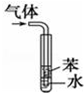 | 用于吸收HCl气体能防倒吸 |
| A. | A | B. | B | C. | C | D. | D |
12.在一定温度下,密闭容器中可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A. | C的反应速率与B的生成速率相等 | |
| B. | 单位时间内生成2n mol A,同时生成3n mol B | |
| C. | A、B、C的浓度不再变化 | |
| D. | A、B、C的浓度之比为1:3:2 |
19.下列除杂(括弧内为杂质气体)试剂和方法不正确的是( )
| 序号 | 气体 | 除杂试剂 |
| A | CO2(HCl) | 盛饱和NaHCO3溶液的吸气瓶 |
| B | Cl2(HCl) | 盛饱和食盐水的吸气瓶 |
| C | NH3(H2O) | 盛碱石灰的球形干燥管 |
| D | SO2(HCl) | 盛饱和AgNO3溶液的吸气瓶 |
| A. | A | B. | B | C. | C | D. | D |
13.碳酸钠和碳酸氢钠是生活中常见的盐,下列说法错误的是( )
| A. | 可通入过量的CO2气体来除去NaHCO3溶液中少量的Na2CO3杂质 | |
| B. | 可采用滴加少量的澄清石灰水来鉴别Na2CO3和NaHCO3两种白色固体 | |
| C. | 等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,后者放出的CO2多 | |
| D. | 通过称取ag Na2CO3和NaHCO3的混合物经充分加热冷却后恒重bg能够测出混合物中Na2CO3的质量分数 |
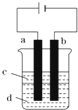 Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.
Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.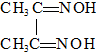 )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.