题目内容
将十水碳酸钠与碳酸氢钠的混合物4.54g溶于水,配成100ml溶液.测得溶液中钠离子的物质的量浓度为0.4mol/L,在溶液中加入过量的盐酸,完全反应后,将溶液蒸干灼烧至质量不变,则所得固体的质量为( )
| A、4.54g |
| B、3.34g |
| C、2.57g |
| D、2.34g |
考点:有关混合物反应的计算
专题:计算题
分析:在溶液中加入过量的盐酸,完全反应后,将溶液蒸干灼烧至质量不变,则所得固体为氯化钠,根据元素守恒以及m=nM计算氯化钠的质量.
解答:
解:溶液中Na+的物质的量为0.1L×0.4mol/L=0.04mol;根据钠离子守恒,n( Na元素)=0.04mol,n(NaCl)=0.04mol,在溶液中加入过量的盐酸,完全反应后,将溶液蒸干灼烧至质量不变,则所得固体为氯化钠,质量是0.04mol×58.5g/mol=2.34g,
故选D.
故选D.
点评:本题考查混合物计算,难度不大,明确发生的反应是关键,注意利用钠元素守恒计算.

练习册系列答案
相关题目
下列反应中,属于加成反应的是( )
| A、乙烯使溴水褪色 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、乙烯在空气中燃烧 |
| D、苯在浓硫酸条件下与浓硝酸共热 |
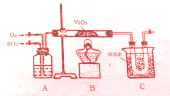 某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答:
某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答: