题目内容
0.035mol铜完全溶于硝酸,产生氮的氧化物(NO、NO2、N2O4)混合气体共0.05mol.该混合气体的平均相对分子质量可能是( )
| A、30 | B、42 | C、45 | D、60 |
考点:氧化还原反应的计算
专题:
分析:Cu-2e=Cu2+,0.035mol铜完全溶于硝酸失去电子为0.07mol,根据氧化还原反应电子守恒可知,HNO3→NO2+NO+N2O4,0.05mol氮氧化物共得到0.07mol电子,从两个极端来考虑:(1)假设混合气体为NO、NO2;(2)假设混合气体是N2O4、NO2,据此计算平均相对分子质量,实际混合气体的相对分子质量介于两者之间.
解答:
解:Cu-2e=Cu2+,0.035mol铜完全溶于硝酸失去电子为0.07mol,根据氧化还原反应电子守恒可知,HNO3→NO2+NO+N2O4,0.05mol氮氧化物共得到0.07mol电子,
(1)假设混合气体中没有N2O4时,设NO的物质的量为x,则NO2的物质的量为0.05mol-x,则0.035mol×2=3x+(0.05mol-x)×1,解得:x=0.01mol,NO2的物质的量为0.05mol-0.01mol=0.04mol,所以混合气体的平均相对分子质量为
=42.8;
(2)假设混合体中没有NO时,设N2O4、NO2物质的量分别为m,n,m+n=0.05mol,2m+n=0.07mol,联立解得m=0.02mol,n=0.03mol,所以混合气体的平均相对分子质量为46×
+92×
=73.6,
所以该混合气体的平均相对分子质量应在42.8~73.6之间.
故选CD.
(1)假设混合气体中没有N2O4时,设NO的物质的量为x,则NO2的物质的量为0.05mol-x,则0.035mol×2=3x+(0.05mol-x)×1,解得:x=0.01mol,NO2的物质的量为0.05mol-0.01mol=0.04mol,所以混合气体的平均相对分子质量为
| 30×0.01+46×0.04 |
| 0.05 |
(2)假设混合体中没有NO时,设N2O4、NO2物质的量分别为m,n,m+n=0.05mol,2m+n=0.07mol,联立解得m=0.02mol,n=0.03mol,所以混合气体的平均相对分子质量为46×
| 2 |
| 5 |
| 3 |
| 5 |
所以该混合气体的平均相对分子质量应在42.8~73.6之间.
故选CD.
点评:本题考查氧化还原反应的计算,为高频考点,把握电子守恒及极限法计算为解答的关键,侧重分析与计算能力的考查,题目难度中等.

练习册系列答案
相关题目
相同质量的钠在下列情况下产生氢气最多的是( )
①放在足量水中
②放在足量盐酸中
③放在足量CuSO4溶液中
④用刺有小孔的铝,包好放入足量水底中.
①放在足量水中
②放在足量盐酸中
③放在足量CuSO4溶液中
④用刺有小孔的铝,包好放入足量水底中.
| A、①②④ | B、②③④ |
| C、①③④ | D、④ |
儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用.下列说法正确的是( )
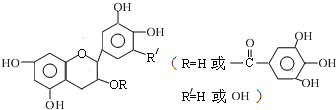

| A、常温下,儿茶素不溶于水,也不溶于有机溶剂 |
| B、儿茶素一定不能发生水解反应 |
| C、1mol儿茶素最少可与5mol NaOH反应 |
| D、儿茶素能与FeCl3溶液发生显色反应 |
下列物质的应用或转化与氧化还原反应原理有关的是( )
| A、工业上用铁矿石炼铁 |
| B、用稀盐酸除去钢铁表面的铁锈 |
| C、工业上煅烧石灰石制生石灰 |
| D、用胃舒平(氢氧化铝)治疗胃酸过多 |
室温下某透明溶液中由水电离产生的H+和OH-浓度的乘积为=1×10-24mol2?L-2,满足此条件的溶液中一定可以大量共存的离子组是( )
| A、MnO4- Na+ SO42-K+ |
| B、Fe2+ Na+ Cl- NO3- |
| C、K+ Na+ Cl- CO32- |
| D、K+ NH4+ SO42- NO3- |
将十水碳酸钠与碳酸氢钠的混合物4.54g溶于水,配成100ml溶液.测得溶液中钠离子的物质的量浓度为0.4mol/L,在溶液中加入过量的盐酸,完全反应后,将溶液蒸干灼烧至质量不变,则所得固体的质量为( )
| A、4.54g |
| B、3.34g |
| C、2.57g |
| D、2.34g |
验证某有机物属于烃的含氧衍生物,应完成的实验内容是( )
| A、只要验证它完全燃烧后产物只有H2O和CO2 |
| B、只要测定其燃烧产物中H2O和CO2物质的量的比值 |
| C、测定该试样的质量及其试样完全燃烧后生成H2O和CO2的质量 |
| D、测定完全燃烧时消耗有机物与生成H2O和CO2的物质的量之比 |
 利用合成氨生产尿素[CO(NH2)2]是重要的化学工艺.在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:3H2(g)+N2(g)?2NH3(g).保持恒温、恒容,测得反应达到平衡时有关数据如下:
利用合成氨生产尿素[CO(NH2)2]是重要的化学工艺.在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:3H2(g)+N2(g)?2NH3(g).保持恒温、恒容,测得反应达到平衡时有关数据如下: